题目内容
1.已知如图是两种元素在周期表中的信息.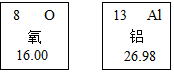
回答下列问题:
(1)金属铁是由原子(填“原子”、“分子”或“离子”,下同)构成的,氯化钠是由离子构成的.
(2)原子得到或失去电子后形成离子.某离子的结构示意图为
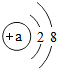
①当a=10时,该粒子是原子,且是稀有气体原子((填“金属”、“非金属”或“稀有气体”)
②当a=8时,该粒子是阴离子(填“原子”、“阳离子”或“阴离子”)其符号为O2-.
分析 (1)根据物质的构成来分析;
(2)根据质子数与核外电子数的关系可知,若质子数等于核外电子数,则为原子,若质子数小于核外电子数,则为阴离子,质子数决定了元素.
解答 解:(1)铁是金属单质,由铁原子构成的;氯化钠是由钠离子和氯离子构成的;故填:原子;离子;
(2)①因该粒子是原子,则a=2+8=10,10号元素是氖元素,属于稀有气体元素;故答案为:10; 稀有气体;
②因核外电子总数2+8,a=8时小于核外电子总数,则为阴离子,因质子数为8,则为氧元素,该离子为带2个单位负电荷的氧离子,离子符号为 O2-,
故答案为:阴离子; O2-.
点评 本题考查物质的构成微粒及原子中的量的关系,明确常见物质的构成微粒,学会利用质子数与核外电子数的关系来分析原子和离子即可解答.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.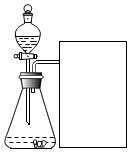 实验室常用过氧化氢溶液和二氧化锰(催化剂)制取氧气.
实验室常用过氧化氢溶液和二氧化锰(催化剂)制取氧气.
【提出问题】催化剂二氧化锰的用量对反应速率是否有影响?
【设计实验】
(1)实验装置如图所示:
(2)实验记录:实验数据如下表:
【实验分析】
(1)过氧化氢分解的文字表达式为过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;二氧化锰可作为该反应的催化剂的依据是能够加快过氧化氢的分解速率,而本身的质量和化学性质在反应前后都不变.
(2)表格中的“测量数据”是:相同时间内收集的氧气体积
(3)本实验中,测定待测数据的装置(图中虚线框里)是c(填编号).
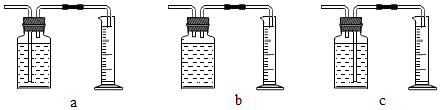
(4)若第Ⅱ次比第Ⅲ次实验的“测量数据”更小(填“大”或“小”)说明催化剂的用量越多,反应更快.
【实验反思】除了上述因素会影响过氧化氢的反应速率外,过氧化氢浓度(写一种)也会影响过氧化氢的分解反应速率,请写出你的实验方案:取相同体积、不同浓度的过氧化氢溶液,分别加入相同质量的二氧化锰,比较相同时间内收集的氧气体积大小.
 实验室常用过氧化氢溶液和二氧化锰(催化剂)制取氧气.
实验室常用过氧化氢溶液和二氧化锰(催化剂)制取氧气.【提出问题】催化剂二氧化锰的用量对反应速率是否有影响?
【设计实验】
(1)实验装置如图所示:
(2)实验记录:实验数据如下表:
| 过氧化氢体积(mL) | 过氧化氢浓度 | 二氧化锰质量(g) | 测量数据(mL) | |
| Ⅰ | 30 | 5% | 0.1 | |
| Ⅱ | 30 | 5% | 0.2 | |
| Ⅲ | 30 | 5% | 0.3 |
(1)过氧化氢分解的文字表达式为过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;二氧化锰可作为该反应的催化剂的依据是能够加快过氧化氢的分解速率,而本身的质量和化学性质在反应前后都不变.
(2)表格中的“测量数据”是:相同时间内收集的氧气体积
(3)本实验中,测定待测数据的装置(图中虚线框里)是c(填编号).

(4)若第Ⅱ次比第Ⅲ次实验的“测量数据”更小(填“大”或“小”)说明催化剂的用量越多,反应更快.
【实验反思】除了上述因素会影响过氧化氢的反应速率外,过氧化氢浓度(写一种)也会影响过氧化氢的分解反应速率,请写出你的实验方案:取相同体积、不同浓度的过氧化氢溶液,分别加入相同质量的二氧化锰,比较相同时间内收集的氧气体积大小.
9.下列有关实验现象描述错误的是( )
| A. | 红磷点燃后伸入氧气中燃烧产生大量的白雾,放热 | |
| B. | 镁条在空气中燃烧发出耀眼的白光,生成固体 | |
| C. | 铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 氢气在空气中燃烧时,发出淡蓝色火焰,放热 |
16.小婧同学学习化学后知道,镁在氧气中燃烧会生成白色的氧化镁固体.但她在空气中点燃镁条时,发现生成的白色固体中还夹杂着少量的淡黄色固体.
【提出问题】为什么会生成淡黄色固体?
【查阅资料】小婧查阅资料,记录了下列几种物质的颜色:
(1)其他同学认为不需要查询氯化镁的颜色,理由是空气中无氯元素.
(2)【提出猜想】分析资料,小茜认为淡黄色固体可能是由镁与空气中的N2反应生成的.
(3)【实验探究】
(4)【拓展应用】若有72g的镁在空气中完全燃烧,则所得含镁元素的产物的总质量范围是100g-120g.
【提出问题】为什么会生成淡黄色固体?
【查阅资料】小婧查阅资料,记录了下列几种物质的颜色:
| 物质 | MgO | MgCl2 | Mg3N2 | Mg(NO2)2 |
| 颜色 | 白色 | 白色 | 淡黄色 | 白色 |
(2)【提出猜想】分析资料,小茜认为淡黄色固体可能是由镁与空气中的N2反应生成的.
(3)【实验探究】
| 实验操作 | 实验现象 | 实验结论和化学方程式 |
| 将点燃的镁条伸入充满氮气的集气瓶中燃烧,观察现象 | 生成淡黄色的固体 | 小茜的猜想成立,化学方程式为 3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2. |
13.如图所示的实验操作中,正确的是( )
| A. |  | B. |  | ||
| C. | 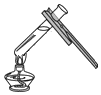 | D. | 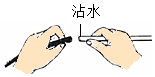 |

