题目内容
11.实验室常用二氧化锰和浓盐酸共热制氯气,反应的化学方程式:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,下列说法正确的是( )| A. | 反应前后锰元素的化合价降低 | |
| B. | 制氯气装置与实验室制取二氧化碳装置完全相同 | |
| C. | 用浓盐酸配制稀盐酸时,必须用托盘天平、量筒、烧杯和玻璃棒 | |
| D. | 该反应是复分解反应 |
分析 制取装置包括加热和不需加热两种,在MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O中,反应前后锰元素的化合价由+4价变为+2价,化合价降低;制氯气装置与实验室制取二氧化碳装置完全相同错误,制二氧化碳不需要加热,制氯气需要加热;用浓盐酸配制稀盐酸时,必须用量筒、烧杯和玻璃棒,不用托盘天平;该反应不属于复分解反应.
解答 解:A、在MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O中,反应前后锰元素的化合价由+4价变为+2价,化合价降低;故选项正确;
B、制氯气装置与实验室制取二氧化碳装置完全相同错误,制二氧化碳不需要加热,制氯气需要加热;故选项错误;
C、用浓盐酸配制稀盐酸时,必须用量筒、烧杯和玻璃棒,不用托盘天平;故选项错误;
D、该反应不属于复分解反应,故选项错误;
故选A
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了反应的类型等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
2.下列实验现象描述中不正确的是( )
| A. | 红磷在空气中燃烧,产生大量白烟 | |
| B. | 向NaOH溶液中滴加酚酞,溶液变红 | |
| C. | 细铁丝在空气中燃烧,火星四射,生成黑色固体 | |
| D. | 把铝片浸入CuSO4溶液中,一段时间后取出,铝片表面覆盖一层红色物质 |
19.将100mL水和100mL酒精混合,其总体积会( )
| A. | 小于200mL | B. | 大于200mL | C. | 等于200mL | D. | 无法确定 |
3.某兴趣小组同学在探究碱溶液与酚酞作用的实验时,发现了一个意外现象:氢氧化钠溶液滴入酚酞试液中,溶液变成了红色,一会儿红色就消失了.
【猜想】可能与氢氧化钠溶液质量分数大小有关.
【实验设计一】
【反思与评价】
通过大家分析讨论,认为可能还有以下猜想:
猜想一、可能是酚酞变质的缘故;
猜想二、可能是氢氧化钠溶液与空气中二氧化碳反应的缘故;
猜想三、可能是酚酞与空气中氧气反应,使红色消失的缘故. …
【实验设计二】为证实猜想三,做如下实验,请完成下表.
【理论分析】猜想一不对,理由是若酚酞试液变质,就不可能出现遇氢氧化钠溶液变红的现象;
猜想二也不正确,理由是碳酸钠溶液显碱性,也可使酚酞试液变红;
猜想三也不正确,理由是实验过程中试液一直与氧气接触.
【猜想】可能与氢氧化钠溶液质量分数大小有关.
【实验设计一】
| 实验方法 | 观察到的现象和结论 |
| 分别配制不同质量分数的氢氧化钠溶液,然后各滴加2滴酚酞试液. | 质量分数小的溶液中红色不消失,质量分数大的溶液中红色会消失,则证明与NaOH溶液质量分数大小有关. |
通过大家分析讨论,认为可能还有以下猜想:
猜想一、可能是酚酞变质的缘故;
猜想二、可能是氢氧化钠溶液与空气中二氧化碳反应的缘故;
猜想三、可能是酚酞与空气中氧气反应,使红色消失的缘故. …
【实验设计二】为证实猜想三,做如下实验,请完成下表.
| 实验步骤 | 设计这一步骤的目的 |
| 1.用煮沸过的蒸馏水配制氢氧化钠溶液. | 排除水中溶解的O2 |
| 2.在氢氧化钠溶液中滴入酚酞,并在上 方滴一些植物油. | 隔绝O2 |
猜想二也不正确,理由是碳酸钠溶液显碱性,也可使酚酞试液变红;
猜想三也不正确,理由是实验过程中试液一直与氧气接触.
20.化学课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,开展了以下探究:
[提出问题1]该氢氧化钠溶液是否变质了呢?
[实验探究1]
[提出问题2]该氢氧化钠溶液是全部变质还是部分变质呢?
[猜想与假设]猜想1:氢氧化钠溶液部分变质.
猜想2:氢氧化钠溶液全部变质.
[查阅资料](1)氯化钙溶液呈中性.
(2)氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3═CaCO3↓+2NaCl
[实验探究2]
[实验结论]该氢氧化钠溶液部分(填“部分”或“全部”)变质.
[反思与评价]
(1)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式:CO2+2NaOH=Na2CO3+H2O.
(2)在上述[实验探究2]中,小明提出可用氢氧化钙溶液代替X溶液,你认为该方案不可行(填“可行”或“不可行”).
[提出问题1]该氢氧化钠溶液是否变质了呢?
[实验探究1]
| 实验操作 | 实验现象 | 实验结论 |
| 取少量该溶液于试管中,向溶液中滴加稀盐酸,并不断振荡. | 有气泡产生. | 氢氧化钠溶液一定变质了. |
[猜想与假设]猜想1:氢氧化钠溶液部分变质.
猜想2:氢氧化钠溶液全部变质.
[查阅资料](1)氯化钙溶液呈中性.
(2)氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3═CaCO3↓+2NaCl
[实验探究2]
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量该溶液于试管中,向溶液中滴加过量的X氯化钙溶液,并不断振荡. | 有白色沉淀生成. | 说明原溶液中一定有碳酸钠. |
| (2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液. | 溶液变红色. | 说明原溶液中一定有氢氧化钠. |
[反思与评价]
(1)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式:CO2+2NaOH=Na2CO3+H2O.
(2)在上述[实验探究2]中,小明提出可用氢氧化钙溶液代替X溶液,你认为该方案不可行(填“可行”或“不可行”).
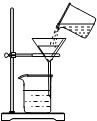 某同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉未搅拌溶解,静置一会儿后,采用如图所示装置进行过滤,请问:
某同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉未搅拌溶解,静置一会儿后,采用如图所示装置进行过滤,请问:
