题目内容
3.在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示,下列说法不正确的是( )
| A. | 丙一定是化合物 | |
| B. | 在该反应中丁可能参加化学反应 | |
| C. | 该反应是化合反应 | |
| D. | 甲和乙的质量之和一定等于生成丙的质量 |
分析 反应后质量增加的物质是生成物,反应后质量减少的物质是反应物,反应前后质量不变的物质可能是催化剂,也可能既不是反应物,也不是生成物,也不是催化剂.
解答 解:反应前后容器中物质的总质量不变,反应后质量分数减小的物质是反应物,质量分数增大的物质是生成物,由图中物质的质量分数的变化可知,甲和乙的质量分数减小,是反应物,丙物质的质量分数增大,是生成物,而丁物质的质量分数不变,丁物质可能是催化剂;
A、由以上分析可知,甲和乙物质反应生成了丙物质,属于化合反应,丙物质属于化合物,故说法正确.
B、丁物质的质量分数不变,丁物质可能是催化剂,可能参加化学反应,故说法正确.
C、反应物是两种,生成物是一种,属于化合反应,故说法正确.
D、应该是参加反应的甲和乙的质量之和一定等于生成丙的质量,甲物质和乙物质没有完全反应,故说法错误.
故选:D.
点评 理解质量守恒定律时,要注意是参加反应的物质的质量等于反应后生成的物质的质量,没有参与反应的那部分物质的质量不能计算在内.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
13.下列反应中,既不属于化合反应也不属于分解反应的是( )
| A. | 碱式碳酸铜$\stackrel{加热}{→}$氧化铜+二氧化铜+水 | |
| B. | 酒精+氧气$\stackrel{点燃}{→}$二氧化碳+水 | |
| C. | 镁+氧气$\stackrel{点燃}{→}$氧化镁 | |
| D. | 铁+氧气$\stackrel{点燃}{→}$四氧化三铁 |
18.钚除用于核电外,还可用于制造核武器,钚元素的有关信息如图,下列说法正确的是( )
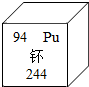

| A. | 钚原子中有94个中子 | B. | 钚原子核外有150个电子 | ||
| C. | 钚的相对原子质量是244g | D. | 钚是金属元素 |
8.人类生存离不开空气,下列说法正确的是( )
| A. | 空气中可吸入颗粒物(PM2.5)的多少不影响人体健康 | |
| B. | 空气是由多种物质组成的混合物 | |
| C. | 空气中二氧化碳的体积只占0.03%,因此它的作用很小 | |
| D. | 空气中氮气的质量分数为78% |
15.关于100克5%的氯化钠溶液,下列叙述错误的是( )
| A. | 100克水中溶有5克氯化钠 | B. | 5克氯化钠溶于95克水中 | ||
| C. | 溶质与溶液的质量比为1:20 | D. | 溶质与溶剂的质量比为1:19 |
12.某同学分别各取四份50g的水,再分别加入一定质量的硝酸钾固体,配制成一定温度下的溶液,充分搅拌后,滤去未溶解的固体,将相关数据记录如表:
根据以上数据,请回答:
(1)①得到的溶液一定不是饱和溶液(选填“一定”、“不一定”、“一定不”之一),
③得到的溶液一定是饱和溶液(选填“一定”、“不一定”、“一定不”之一);
(2)列式计算④所得溶液中溶质的质量分数为多少?
| 操作序号 | ① | ② | ③ | ④ |
| 加入硝酸钾质量/g | 30 | 40 | 50 | 60 |
| 溶液质量/g | 80 | 90 | 100 | 100 |
(1)①得到的溶液一定不是饱和溶液(选填“一定”、“不一定”、“一定不”之一),
③得到的溶液一定是饱和溶液(选填“一定”、“不一定”、“一定不”之一);
(2)列式计算④所得溶液中溶质的质量分数为多少?
13.泰安酿酒厂广告词“金泰山银泰山,开坛飘香醉人间”,其中的化学原理是( )
| A. | 分子是由原子构成的 | B. | 分子间是有间隔的 | ||
| C. | 分子是不断运动的 | D. | 分子间存在相互作用 |
