题目内容
3.镁是一种用途很广的金属,目前世界上60%的镁是从海水(主要含NaCl和MgCl2等)中提取的,主要步骤如下:
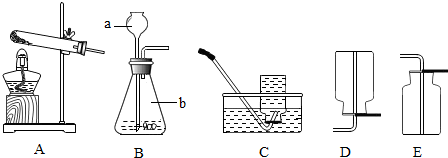
(1)实验步骤①操作后得到的溶液仍然浑浊的原因可能是什么?
(2)步骤①和步骤③的实验操作都用到一种玻璃仪器,该仪器在操作步骤③中的作用是什么?
(3)请写出沉淀B与试剂C发生中和反应的化学方程式.
分析 (1)滤纸破损、液面超过滤纸边缘、接滤液的烧杯不干净等都可以导致滤液仍然浑浊;
(2)根据玻璃棒的作用来分析;
(3)海水中含有氯化镁,氯化镁与氢氧化钙反应生成氢氧化镁沉淀和氯化钙,沉淀B为氢氧化镁,氢氧化镁与稀盐酸发生中和反应生成氯化镁和水,写出反应的化学方程式即可.
解答 解:(1)如经过滤后,滤液仍然浑浊,则可能的原因是:滤纸破损或液面高于滤纸边缘或仪器不干净;故填:滤纸破损(或液面高于滤纸的边缘或玻璃仪器不干净);
(2)步骤③是蒸发结晶的过程,此过程中玻璃棒的作用是搅拌,防止局部受热过高造成液体飞溅;故填:搅拌,防止局部受热过高造成液体飞溅;
(3)海水中含有氯化镁,氯化镁与氢氧化钙反应生成氢氧化镁沉淀和氯化钙,沉淀B为氢氧化镁,氢氧化镁与稀盐酸发生中和反应生成氯化镁和水,反应的化学方程式为Mg(OH)2+2HCl═MgCl2+2H2O.故填:Mg(OH)2+2HCl═MgCl2+2H2O.
点评 本题难度不大,掌握海水中提取镁的原理、盐的化学性质、化学方程式的书写方法等是正确解答本题的关键.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
4.下列变化为属于化学变化的是( )
| A. | 汽油挥发 | B. | 干冰升华 | C. | 粮食酿酒 | D. | 蜡烛熔化 |
14.下列说法中一定正确的是( )
| A. | 单质由一种元素组成,由一种元素组成的物质不一定是单质 | |
| B. | 置换反应中有一种单质和一种化合物生成,有一种单项和一种化合物生成的反应不一定是置换反应 | |
| C. | 相同温度下氯化钠饱和溶液的浓度大于不饱和溶液的浓度,所以该温度下氯化钠饱和溶液中的溶质质量也大于不饱和溶液 | |
| D. | 锌比铁活泼,所以将等质量的锌粒和铁粉分别放入等质量等质量分数的稀盐酸中,锌粒产生的气泡速率快 |
11.向盛有等量水的①、②、③烧杯中分别加入10g、25g、25gNaNO3固体,充分溶解后,其现象如图一所示.则下列说法错误的是( )


| A. | 烧杯②中的溶液一定属于饱和溶液 | |
| B. | 图二中能表示NaNO3溶解度曲线的是甲 | |
| C. | 分别将100g甲、乙的饱和溶液从t2℃降温到t1℃后,溶液中所含溶剂质量关系为甲=乙 | |
| D. | t1℃甲、乙饱和溶液的溶质质量分数一定相等 |
15.下列有关溶液的说法正确的是( )
| A. | 溶液一定是混合物 | |
| B. | 凡是均一、稳定的液体都是溶液 | |
| C. | 一定温度下的饱和溶液中不能溶解任何物质 | |
| D. | 一种物质分散到另一种物质中形成的液体是溶液 |
 已知A、B、C、D、E是初中化学中常见的五种物质,均含碳元素.其中,只有A为单质,B和C是含有相同元素的氧化物,D与其它四种物质属于不同的类别,E是大理石的主要成分,它们在一定条件下的转化关系如图所示(反应条件和部分反应物、生成物已省略),请回答:
已知A、B、C、D、E是初中化学中常见的五种物质,均含碳元素.其中,只有A为单质,B和C是含有相同元素的氧化物,D与其它四种物质属于不同的类别,E是大理石的主要成分,它们在一定条件下的转化关系如图所示(反应条件和部分反应物、生成物已省略),请回答: