题目内容
2.运载火箭的动力可由高氯酸铵(NH4CLO4)分解提供,化学方程式为2NH4CLO4?N2↑+Cl2↑+4X↑+2O2↑.下列有关说法不正确的是( )| A. | X的化学式为H2O | |
| B. | 该反应属于分解反应 | |
| C. | NH4CLO4中氯元素的化合价为+7 | |
| D. | 反应生成氮气和氧气的质量比为7:8 |
分析 A.根据化学变化前后原子的种类、数目不变,由反应的化学方程式2NH4ClO4$\frac{\underline{\;\;△\;\;}}{\;}$N2↑+Cl2↑+4X↑+2O2↑,推断反应中生成物X的分子构成,然后确定X物质的化学式.
B.根据分解反应的定义分析解答;
C.根据化合物中正负化合价代数和为零解答;
D.根据生成的氮气和氧气的质量比来分析解答;
解答 解:A.由反应的化学方程式2NH4ClO4$\frac{\underline{\;\;△\;\;}}{\;}$N2↑+Cl2↑+4X↑+2O2↑,可知:
反应前 反应后
N原子 2 2
H原子 8 0
Cl原子 2 2
O原子 8 4
根据化学变化前后原子的种类、数目不变,可判断生成物X的4个分子中含有8个H原子和4个O原子,则每个X的分子由2个H原子和1个O原子构成,物质X的化学式为H2O,正确;
B.根据化学反应化学方程式为2NH4Cl04$\frac{\underline{\;\;△\;\;}}{\;}$N2↑+Cl2↑+4X↑+202↑,可知该反应为“一分多”是分解反应,正确;
C.铵根显+1价,氧元素显-2价,设氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(-2)×4=0,则x=+7价;正确;
D.生成的氮气和氧气的质量比为:14×2:16×2×2=7:16;错误;
答案:B
点评 根据化学变化前后原子的种类、数目不变,由反应的化学方程式,可以推断反应中某物质的分子构成及物质化学式的确定.

练习册系列答案
 综合自测系列答案
综合自测系列答案
相关题目
12.下列实验操作正确的是( )
| A. |  滴加液体 | B. |  测定溶液PH | C. | 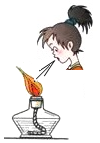 熄灭酒精灯 | D. | 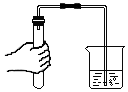 检查装置气密性 |
13.如图是甲、乙、丙三种物质的溶解度曲线,下列说法正确的是( )
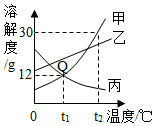

| A. | 将丙的饱和溶液变为不饱和溶液,可采用升温的方法 | |
| B. | t1℃时,可以制得溶质质量分数为8%的丙溶液 | |
| C. | t2℃时,甲、乙两种物质的饱和溶液降温至20℃,析出甲的质量比析出乙的质量大 | |
| D. | t1℃时甲、乙、丙三种物质的饱和溶液升高到t2℃时,溶质质量分数为甲>乙>丙 |
17.碳酸钠是重要的化工原料,其俗称为( )
| A. | 小苏打 | B. | 纯碱 | C. | 烧碱 | D. | 火碱 |
7.下列试剂中,能把稀硫酸、KOH溶液、CaCl2溶液一次性鉴别出来的是( )
| A. | KCl溶液 | B. | K2CO3溶液 | C. | 稀盐酸 | D. | 酚酞溶液 |
1.正确量取45mL液体,应选用的一组仪器是( )
①100mL量筒②10mL量筒③50mL量筒④胶头滴管.
①100mL量筒②10mL量筒③50mL量筒④胶头滴管.
| A. | ③④ | B. | ①②④ | C. | ③ | D. | ②④ |
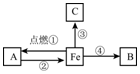 如图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质),其中B是密度最小的气体,C为红色固体单质.
如图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质),其中B是密度最小的气体,C为红色固体单质.