题目内容
12.将25g硝酸钾溶于100g水里,所得溶液均匀分为五等分:(1)每一份溶液中KNO3的质量分数为20%;
(2)向第一份溶液中加入15g水后,溶液中KNO3的质量分数为12.5%;
(3)向第二份溶液中加入15g KNO3并全部溶解,所得溶液中KNO3的质量分数为50%;
(4)若将第三份溶液变为10%溶液,可采取的措施是加入25g水;
(5)若将第四份溶液变为40%溶液,可加热蒸发掉12.5g水(无晶体析出).
分析 (1)根据溶质的质量分数计算方法来分析;
(2)根据溶质的质量不变,溶剂的质量增加来分析;
(3)根据溶剂的质量不变,溶质的质量增加来分析;
(4)可通过加入水的方法使溶液的浓度减小;
(5)根据蒸发水的过程中溶质的质量不变来分析.
解答 解:(1)由于溶液的均一性,每一份溶液中KNO3的质量分数与整体的质量分数相同,溶质的质量分数=$\frac{溶质的质量}{溶液的质量}$×100%=$\frac{25g}{25g+100g}$×100%=20%,故填:20%;
(2)均分为五等份后,每份中有5g溶质,20g溶剂.则向第一份溶液中加入15g水后,溶液中KNO3的质量分数为:$\frac{5g}{25g+15g}$×100%=12.5%,故填:12.5%;
(3)向第二份溶液中加15gKNO3并全部溶解,所得溶液中KNO3的质量分数为:$\frac{5g+15g}{25g+15g}×100%$=50%,故填:50%;
(4)设加水的质量为x,则$\frac{5g}{25g+x}×100%$=10%
x=25g
故填:加入25g水;
(5)设蒸发水的质量为y,则$\frac{5g}{25g-y}$×100%=40%
y=12.5g
故填:12.5.
点评 本题考查增大溶质质量分数的方法及有关计算,明确溶液中的变化并学会利用溶质的质量关系来列等式计算是解答的关键.

练习册系列答案
相关题目
3.已基本干燥的抹灰白墙(熟石灰),住人后往往又会变得潮湿,这主要是由于( )
| A. | 壁中有水渗出 | |
| B. | 熟石灰与二氧化碳反应的生成物中有水 | |
| C. | 空气中的水凝结在墙面 | |
| D. | 熟石灰变成了生石灰和水 |
20.下列对生活中一些物质的类别描述不正确的是( )
| A. | 食盐是盐 | B. | 纯碱是碱 | C. | 醋酸是酸 | D. | 水是氧化物 |
7.根据溶液的组成填写如表
| 溶液 | 碘酒 | 石灰水 | 稀硫酸 | |
| 溶质 | 硫酸铜 | |||
| 溶剂 | 水 |
4.下列生活中的变化属于物理变化的是( )
| A. | 食物变质 | B. | 菜刀生锈 | C. | 燃放烟火 | D. | 湿衣服晒干 |
2.从化学的角度看,下列说法中正确的是( )
| A. | 夜晚发现液化气泄漏立即开灯检查 | |
| B. | 化学反应都放热 | |
| C. | 扑灭图书档案等火灾最适宜的灭火器是液态二氧化碳灭火器 | |
| D. | 炒菜时油锅着火,可立即加水灭火 |
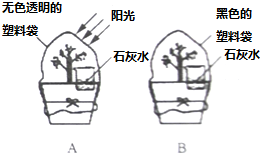 探究植物光合作用与呼吸作用的区别.植物不但进行光合作用,也同时进行呼吸作用.为了比较二者的不同,有人设计了如下实验.在一晴朗的早晨,选取大小相似的同种植物两盆,在花盆上各放一杯澄清石灰水,然后把其中一盆用无色透明的塑料袋罩住,放在阳光下;另一盆则用黑色塑料袋罩住,放在阴暗处(见图).傍晚,在塑料袋上都剪一小口,并插入燃着的木条实验,发现A中木条比B中更亮;而A中石灰水保持澄清,B中变浑浊.
探究植物光合作用与呼吸作用的区别.植物不但进行光合作用,也同时进行呼吸作用.为了比较二者的不同,有人设计了如下实验.在一晴朗的早晨,选取大小相似的同种植物两盆,在花盆上各放一杯澄清石灰水,然后把其中一盆用无色透明的塑料袋罩住,放在阳光下;另一盆则用黑色塑料袋罩住,放在阴暗处(见图).傍晚,在塑料袋上都剪一小口,并插入燃着的木条实验,发现A中木条比B中更亮;而A中石灰水保持澄清,B中变浑浊.