题目内容
9.海水中蕴含着丰富的资源,从海水中获取金属镁的工业流程如下.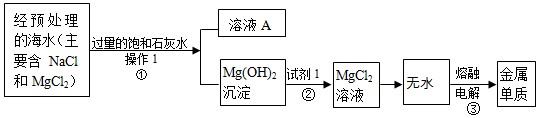
(1)若②发生了中和反应,则试剂1为稀盐酸.
(2)反应③属于分解反应.(填基本反应类型)
分析 氯化镁和氢氧化钙反应生成氢氧化镁沉淀和氯化钙;
氢氧化镁和稀盐酸反应生成氯化镁和水,属于中和反应;
通电条件下,氯化镁分解生成镁和氯气,属于分解反应.
解答 解:(1)若②发生了中和反应,则试剂1为稀盐酸,这是因为氢氧化镁和稀盐酸反应生成氯化镁和水,属于中和反应.
故填:稀盐酸.
(2)反应③中,氯化镁分解生成镁和氯气,属于分解反应.
故填:分解.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
4.浩瀚的大海里蕴藏着丰富的资源,开发海水资源前景广阔.
(1)工业上利用太阳能进行海水晒盐.已知海水蒸发浓缩过程中析出盐的种类和质量如右表:(表中数据为每升海水在浓缩过程中析出各种盐的质量,单位为g)
①海水从密度为1.21g/ml浓缩到1.22g/ml时下列说法正确的是C
A.各种盐的溶解度增大 B.海水中NaBr的质量分数不变
C.析出粗盐中NaCl的质量分数增大 D.海水中水的质量分数不变
②海水在浓缩过程中,最先析出的盐是硫酸钙.
(2)工业上利用粗盐水(含有少量CaCl2、MgCl2)生产纯碱,工艺流程如图:

已知:ⅰ常温下,NH3极易溶于水,CO2能溶于水;
ⅱNaHCO3加热易分解,Na2CO3加热不易分解.
完成下列填空:
①粗盐水加入沉淀剂NaOH、Na2CO3分别除去MgCl2、CaCl2,固体C为Mg(OH)2、CaCO3;
②流程中,先“氨化”后“碳酸化”的目的是氨盐水显碱性,更容易吸收二氧化碳;
③“碳酸化”后过滤获得的NH4Cl可用作氮肥,也可先加热(填“加热”或“冷却”)NH4Cl溶液,再加入石灰水以循环使用的物质是氨气;
④“煅烧”时,NaHCO3分解生成的气体D是二氧化碳,若将气体D直接排入空气不合理的理由是导致温室效应.
(3)海滨研究所以含有CaCl2、MgCl2的卤水和贝壳(主要成分为CaCO3)为主要原料在实验室制备无水CaCl2,流程如图1: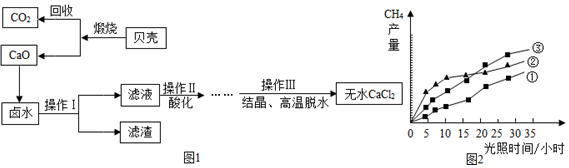
请回答下列问题:
①操作Ⅰ中用到的玻璃仪器有烧杯、玻璃棒、漏斗.
②以MgCl2为例写出卤水中除去Mg2+时发生反应的化学方程式Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2.
③操作Ⅱ酸化时应选择的酸是HCl(填写化学式).
④上述反应中未涉及的基本反应类型是b(填写字母).
a.复分解反应 b.置换反应 c.化合反应 d.分解反应
⑤回收的CO2在紫外线照射和催化剂作用下能与水蒸气反应,生成甲烷和氧气,该反应的化学方程式为CO2+2H2O$\frac{\underline{\;催化剂\;}}{紫外线}$CH4+2O2.紫外线照射时,在不同催化剂(①、②、③)的作用下,甲烷产量随光照时间的变化如图2所示,在第10小时时甲烷产量最高是②(填写“①”、“②”、或“③”).
| 海水密度 | CaSO4 | NaCl | MgCl2 | MgSO4 | NaBr |
| 1.13 | 0.56 | ||||
| 1.20 | 0.91 | ||||
| 1.21 | 0.05 | 3.26 | 0.004 | 0.008 | |
| 1.22 | 0.015 | 9.65 | 0.01 | 0.04 | |
| 1.26 | 0.01 | 2.64 | 0.02 | 0.02 | 0.04 |
| 1.31 | 1.40 | 0.54 | 0.03 | 0.06 |
①海水从密度为1.21g/ml浓缩到1.22g/ml时下列说法正确的是C
A.各种盐的溶解度增大 B.海水中NaBr的质量分数不变
C.析出粗盐中NaCl的质量分数增大 D.海水中水的质量分数不变
②海水在浓缩过程中,最先析出的盐是硫酸钙.
(2)工业上利用粗盐水(含有少量CaCl2、MgCl2)生产纯碱,工艺流程如图:

已知:ⅰ常温下,NH3极易溶于水,CO2能溶于水;
ⅱNaHCO3加热易分解,Na2CO3加热不易分解.
完成下列填空:
①粗盐水加入沉淀剂NaOH、Na2CO3分别除去MgCl2、CaCl2,固体C为Mg(OH)2、CaCO3;
②流程中,先“氨化”后“碳酸化”的目的是氨盐水显碱性,更容易吸收二氧化碳;
③“碳酸化”后过滤获得的NH4Cl可用作氮肥,也可先加热(填“加热”或“冷却”)NH4Cl溶液,再加入石灰水以循环使用的物质是氨气;
④“煅烧”时,NaHCO3分解生成的气体D是二氧化碳,若将气体D直接排入空气不合理的理由是导致温室效应.
(3)海滨研究所以含有CaCl2、MgCl2的卤水和贝壳(主要成分为CaCO3)为主要原料在实验室制备无水CaCl2,流程如图1:

请回答下列问题:
①操作Ⅰ中用到的玻璃仪器有烧杯、玻璃棒、漏斗.
②以MgCl2为例写出卤水中除去Mg2+时发生反应的化学方程式Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2.
③操作Ⅱ酸化时应选择的酸是HCl(填写化学式).
④上述反应中未涉及的基本反应类型是b(填写字母).
a.复分解反应 b.置换反应 c.化合反应 d.分解反应
⑤回收的CO2在紫外线照射和催化剂作用下能与水蒸气反应,生成甲烷和氧气,该反应的化学方程式为CO2+2H2O$\frac{\underline{\;催化剂\;}}{紫外线}$CH4+2O2.紫外线照射时,在不同催化剂(①、②、③)的作用下,甲烷产量随光照时间的变化如图2所示,在第10小时时甲烷产量最高是②(填写“①”、“②”、或“③”).
19.化学概念在逻辑上存在如图所示关系,对下列概念间的逻辑关系说法错误的是( )


| A. | 复分解反应与中和反应属于包含关系 | |
| B. | 含氧的化合物与盐属于交叉关系 | |
| C. | 化合物与氧化物属于交叉关系 | |
| D. | 纯净物与单质属于包含关系 |
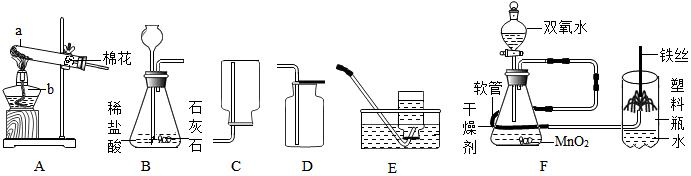
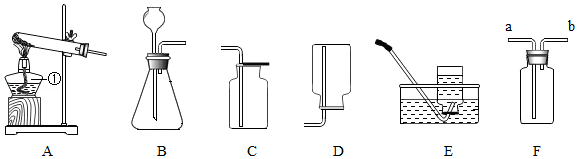
 某化学兴趣小组同学设计了如图所示的装置,请根据所学知识回答有关问题:
某化学兴趣小组同学设计了如图所示的装置,请根据所学知识回答有关问题: