题目内容
实验室做完学生实验后留下含有硝酸银和硝酸铜的混合废液,为了不污染环境,加入铁粉做处理后再倾倒.下列确定硝酸银和硝酸铜已经完全处理的现象为( )
| A、取上层液体加入稀盐酸有白色沉淀 |
| B、取上层液体加入稀盐酸无白色沉淀 |
| C、取底部固体物质加入盐酸有气泡冒出 |
| D、观察上层液体为无色 |
考点:金属的化学性质
专题:金属与金属材料
分析:根据题意,加入铁粉处理学生实验后留下含有硝酸银和硝酸铜的混合废液,铁的金属活动性比铜、银强,能与硝酸银和硝酸铜溶液发生置换反应,完全反应后,可根据铁粉是否有剩余,判断是否已经完全处理.
解答:解:A、稀盐酸与硝酸银溶液反应生成氯化银白色沉淀,取上层液体加入稀盐酸有白色沉淀,说明溶液中存在硝酸银溶液,说明没有完全处理,故选项错误.
B、取上层液体加入稀盐酸无白色沉淀,溶液中也可能存在硝酸铜溶液,不一定说明已经完全处理,故选项错误.
C、加入铁粉处理学生实验后留下含有硝酸银和硝酸铜的混合废液,铁的金属活动性比铜、银强,能与硝酸银和硝酸铜溶液发生置换反应,分别生成硝酸亚铁和铜、硝酸亚铁和银,故处理时可加入过量的铁粉,确定硝酸银和硝酸铜已经完全处理,可根据完全反应后铁粉有剩余;铁能与稀盐酸反应生成氢气,故可取底部固体物质加入盐酸,若有气泡冒出,说明硝酸银和硝酸铜已经完全处理;故选项正确.
D、完全反应后生成的硝酸亚铁溶液呈浅绿色,上层液体不可能为无色,故选项错误.
故选:C.
B、取上层液体加入稀盐酸无白色沉淀,溶液中也可能存在硝酸铜溶液,不一定说明已经完全处理,故选项错误.
C、加入铁粉处理学生实验后留下含有硝酸银和硝酸铜的混合废液,铁的金属活动性比铜、银强,能与硝酸银和硝酸铜溶液发生置换反应,分别生成硝酸亚铁和铜、硝酸亚铁和银,故处理时可加入过量的铁粉,确定硝酸银和硝酸铜已经完全处理,可根据完全反应后铁粉有剩余;铁能与稀盐酸反应生成氢气,故可取底部固体物质加入盐酸,若有气泡冒出,说明硝酸银和硝酸铜已经完全处理;故选项正确.
D、完全反应后生成的硝酸亚铁溶液呈浅绿色,上层液体不可能为无色,故选项错误.
故选:C.
点评:本题难度不大,掌握金属的化学性质、酸的化学性质并能灵活运用是正确解答本题的关键.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案
相关题目
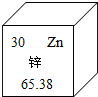 锌对人体健康具有重要意义.在元素周期表中,锌元素的信息如图所示,对图中信息解释不正确的是( )
锌对人体健康具有重要意义.在元素周期表中,锌元素的信息如图所示,对图中信息解释不正确的是( )| A、原子序数为30 |
| B、属于非金属元素 |
| C、元素符号为Zn |
| D、相对原子质量为65.38 |
下列图示的实验中涉及到化学变化的是( )
A、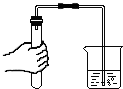 检查装置气密性 |
B、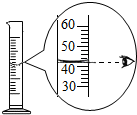 读取水的体积 |
C、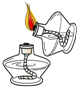 点燃酒精灯 |
D、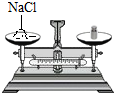 称NaCl的质量 |
下列除杂质的试剂或方法错误的是( )
| A、Cu粉中混有铁粉(硫酸铜溶液) |
| B、CaO中混有CaCO3(稀盐酸) |
| C、C粉中混有CuO(稀硫酸) |
| D、NaNO3溶液中混有NaCl(AgNO3溶液) |
下列变化中,属于化学变化的是( )
| A、浓盐酸挥发 | B、铁丝弯曲 |
| C、木炭燃烧 | D、橙子榨汁 |
如图为A、B、C三种物质的溶解度曲线,下列说法正确的是( )


| A、t2℃时,把20gA物质放入50g水中,所得溶液是不饱和的 |
| B、t1℃时的A、B、C饱和溶液升温到t3℃,A与B溶液一样浓 |
| C、t3℃时,A、B、C三种物质的饱和溶液降温到t1℃,所得三种物质的溶液的溶质质量分数相等 |
| D、t3℃时,A物质饱和溶液的溶质质量分数为50% |

