题目内容
1.如图1是实验室制取氧气或二氧化碳时经常用到的装置,请回答有关问题.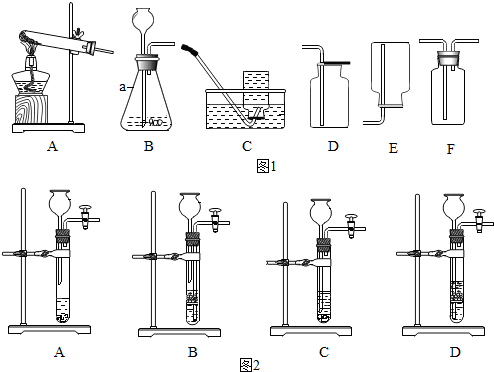
①写出仪器a的名称:锥形瓶;
②实验室用氯酸钾制取干燥的氧气时,可选用的收集装置是D或F(填编号);
③装置B可以用来制取氢气,实验室用锌和稀硫酸制取氢气的反应化学方程式是Zn+H2SO4=ZnSO4+H2↑,,该反应属于置换反应(填化学反应基本类型);
④实验室制取二氧化碳气体时,为了控制反应的发生和停止,可选用图2中的D装置(填编号),选用该发生装置制取气体需满足的一般条件是块状固体和液体反应,反应不需要加热
⑤实验室制取二氧化碳时,所用大理石与100g稀盐酸恰好完全反应(杂质不参与反应),生成8.8g二氧化碳,求大理石中所含碳酸钙的物质的量为0.2mol(根据化学方程式列式计算)
分析 ①识别一些简单仪器.
②实验装置的选择条件及其收集装置的选择条件的区别.
③据实验室制取氢气的原理解答;
④装置不同功能不同;
⑤根据化学反应式计算.
解答 解:①仪器a的名称是锥形瓶;
②验室用氯酸钾制取干燥的氧气时,因密度比空气大,因此采用向上排空气法收集;
③实验室用锌和稀硫酸制取氢气的反应化学方程式是Zn+H2SO4=ZnSO4+H2↑;此反应属于置换反应;
④图2中A、B中中的长颈漏斗末端在液面以上,产生的氢气会从长颈漏斗逸出,因此不能选用,实验室制取二氧化碳气体时,所需药品为块状大理石与稀盐酸反应,D有带孔的塑料板,更容易控制反应的发生和停止;
⑤解:n(CO2)=8.8/44=0.2 mol
设大理石中含碳酸钙的物质的量为X
CaCO3+2HCl→CaCl2+CO2↑+H2O
1 1
X 0.2mol
$\frac{1}{x}$=$\frac{1}{0.2mol}$
X=0.2 mol
答:大理石中含碳酸钙为0.2mol
故答案为:①锥形瓶;②D或F;③Zn+H2SO4=ZnSO4+H2↑,置换反应;
④D、块状固体和液体反应,反应不需要加热;
⑤解:n(CO2)=8.8/44=0.2 mol
设大理石中含碳酸钙的物质的量为X
CaCO3+2HCl→CaCl2+CO2↑+H2O
1 1
X 0.2mol
$\frac{1}{x}$=$\frac{1}{0.2mol}$
X=0.2 mol
答:大理石中含碳酸钙为0.2mol
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案| A. | 蒸馏水 | B. | 矿泉水 | C. | 石灰水 | D. | 汽水 |
| A. | 实验的步骤为计算、称取、量取、溶解、转移 | |
| B. | 溶解过程中玻璃棒的作用是搅拌,以加快氯化钠的溶解速率 | |
| C. | 量取水时,用规格为100mL的量筒量取90mL蒸馏水 | |
| D. | 把配制好的氯化钠溶液倒入刚用蒸馏水洗过的试剂瓶中,贴上标签 |
| A. | 在CO2、SO2、H2O2三种物质中,都含有氧气 | |
| B. | Na和Na+两种微粒中质子数相同,化学性质也相同 | |
| C. | NaOH、Ca(OH)2都是常见的碱,都可用于改良碱性土壤 | |
| D. | 在加热条件下,H2和CO都能使CuO失去氧,H2和CO都发生了氧化反应 |
【提出问题】生成物中有哪种碳的氧化物?
【猜测】
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有CO2 | 含有CO和CO2 |
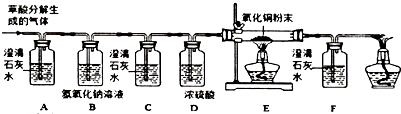
(1)观察到B装置(填字母)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成.
(2)有两种实验现象都能分别证明草酸分解的气体中含有CO;①C装置中澄清石灰水不变浑浊,F中的澄清石灰水变浑浊;②E中的黑色粉末变成红色粉末的现象;
通【实验结论】过实验探究证明:猜想3成立,草酸分解的化学方程式是H2C2O4$\frac{\underline{\;\;△\;\;}}{\;}$CO↑+CO2↑+H2O.
【问题讨论】B装置的作用是吸收二氧化碳气体.
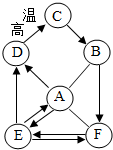 A、B、C、D、E、F均为初中化学中常见的物质,E俗称纯碱,它们之间存在如图的转化关系.“→”表示物质间存在着相应的转化关系,“-”表示物质间能发生反应(部分反应物、生成物和反应条件未标出).
A、B、C、D、E、F均为初中化学中常见的物质,E俗称纯碱,它们之间存在如图的转化关系.“→”表示物质间存在着相应的转化关系,“-”表示物质间能发生反应(部分反应物、生成物和反应条件未标出). 砝码是化学实验室中的常用实验器材,如图所示是一盒砝码的实物图,请你回答下列问题:
砝码是化学实验室中的常用实验器材,如图所示是一盒砝码的实物图,请你回答下列问题: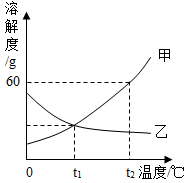 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.