题目内容
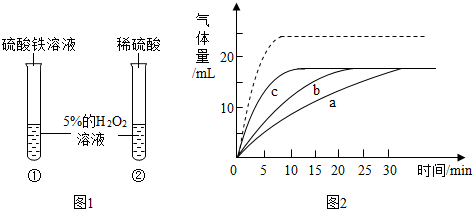
11.课外探究时,某兴趣小组同学选择了“金属和酸反应快慢与什么因素有关”课题.(1)其他条件相同,同种金属与不同质量分数的盐酸反应,反应的快慢不同.取质量相等的铝片,分别放入5%、20%的足量稀盐酸中,实验表明盐酸浓度越大,反应速率越快.如图1中Ⅰ、Ⅱ、Ⅲ是三位同学记录实验生成氢气的质量(m)与反应时间(t)的关系曲线,其中正确的是Ⅲ.
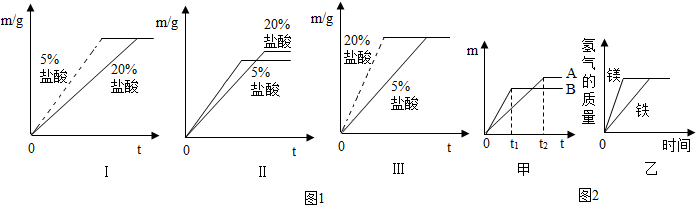
(2)其他条件相同,不同金属与相同质量分数的盐酸反应,反应的快慢不同.取质量相等的镁片、锌片、铁片中的两种金属,分别放入溶质质量分数相同的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系曲线如图甲所示.则曲线A对应的金属与稀盐酸反应后生成的盐的名称是氯化亚铁.
(3)有等质量的镁和铁,镁放入质量分数为10%的稀硫酸中,铁放入质量分数为10%的稀盐酸中,产生氢气的质量随反应时间变化曲线如图乙所示.下列结果可能的是①④(填序号).
①反应后镁有剩余 ②反应后铁有剩余
③反应后稀硫酸有剩余 ④反应后稀盐酸有剩余
⑤剩余铁的和镁的质量相等 ⑥消耗的稀硫酸和稀盐酸质量相等.
分析 (1)根据反应物种类相同时反应物浓度高反应速率快,20%的盐酸比5%的盐酸反应速率快分析;
(2)依据金属活动性顺序及同价态金属与酸反应时生成的氢气量与其相对原子质量呈反比分析判断;
(3)根据金属与酸反应的程度结合图象进行分析解答.
解答 解:(1)反应物种类相同时反应物浓度高反应速率快,20%的盐酸比5%的盐酸反应速率快,取质量相同的锌片生成的氢气质量相同,观察坐标,Ⅲ正确;故填:Ⅲ;
(2)依据金属活动性顺序表可知镁的活动性比锌强,锌的活动性比铁强,同价态三种金属与酸反应时生成的氢气量与其相对原子质量呈反比,所以取质量相等的镁片、铁片和锌片,分别放入溶质质量分数相同的足量稀盐酸中时镁产生的氢气最多,锌生成的氢气量小,因此镁反应的特点是“快而多”,坐标中没有体现出来镁的坐标;锌和铁对比,可知锌反应的特点是快而少,所以B是锌,A是铁,铁和盐酸反应产生氯化亚铁和氢气;故填:氯化亚铁;
(3)根据图示可以看出,最终生成的氢气的质量相等;
Mg+H2SO4═MgSO4+H2↑
24 98 2
Fe+2HCl═FeCl2+H2↑
56 73 2
根据反应的化学方程式以及各物质之间的质量关系可以看出,产生相同质量的氢气,消耗镁的质量小,故镁可能剩余;产生相同质量的氢气,消耗盐酸的质量小,故盐酸可能剩余;故填:①④.
点评 该题通过锌、铁、镁与盐酸之间的反应主要是考查了金属与酸的反应,只要掌握了金属与酸的反应规律以及控制变量法进行实验,便能顺利解题.

练习册系列答案
相关题目
19.小明和同学们做了实验室炼铁的实验.

(1)实验前应先做的是检查装置的气密性.
(2)实验中可观察到的现象是红色固体变黑,澄清的石灰水变浑浊,尾气燃烧,产生蓝色火焰.
(3)小龙认为刚通入CO时不能马上进行尾气处理,这样不安全,他的理由是装置中含有空气,此时的尾气中含有空气,点燃含有空气的一氧化碳时易发生爆炸.
小丽用上述实验中得到的铁与过量的硫酸铜溶液反应,结果发现有部分黑色固体剩余,于是提出了疑问:
【提出问题】炼铁过程中除了生成铁以外还生成了什么?
【查阅质量】
①铁在高温条件下可与水蒸气反应生成一种铁的氧化物和氢气.
②铁和铁的氧化物中只有铁、Fe3O4能被磁铁吸引.
【猜想与假设】
①可能是FeO;
②可能是Fe2O3;
③可能是Fe3O4.
【实验探究】
(4)小丽马上排除了猜想②,理由是Fe2O3是红色粉末.
(5)写出生成该黑色固体的化学方程式3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.

(1)实验前应先做的是检查装置的气密性.
(2)实验中可观察到的现象是红色固体变黑,澄清的石灰水变浑浊,尾气燃烧,产生蓝色火焰.
(3)小龙认为刚通入CO时不能马上进行尾气处理,这样不安全,他的理由是装置中含有空气,此时的尾气中含有空气,点燃含有空气的一氧化碳时易发生爆炸.
小丽用上述实验中得到的铁与过量的硫酸铜溶液反应,结果发现有部分黑色固体剩余,于是提出了疑问:
【提出问题】炼铁过程中除了生成铁以外还生成了什么?
【查阅质量】
①铁在高温条件下可与水蒸气反应生成一种铁的氧化物和氢气.
②铁和铁的氧化物中只有铁、Fe3O4能被磁铁吸引.
【猜想与假设】
①可能是FeO;
②可能是Fe2O3;
③可能是Fe3O4.
【实验探究】
(4)小丽马上排除了猜想②,理由是Fe2O3是红色粉末.
| 实验方案 | 现象与结论 |
| 观察到黑色粉末全部被磁铁吸引,说明猜想③正确. | |
6.随着人们对酒驾危害认识的加深,司法机关对于酒驾、醉驾的处罚将日趋加重.醉酒的原因是酒中含有的乙醇对人的神经系统有刺激作用.交警对呼气酒精检验的原理是:
白酒是乙醇的水溶液,酒中的乙醇在微生物作用下能被氧化成乙酸.小刚家有一瓶密封存放的白酒,他想知道该白酒的组成情况,于是进行如下实验探究:
【提出问题】该白酒中的溶质主要有哪些?
【查阅资料】
材料一:乙醇(C2H5OH),俗称酒精,易溶于水,水溶液呈中性.在加热条件下,可以把氧化铜还原为单质铜.
材料二:乙酸(CH3COOH),又名醋酸,易溶于水,具有酸的通性.
【提出猜想】
猜想1:只有乙醇
猜想2:只有乙酸
猜想3:乙醇和乙酸.
【实验探究】
【实验反思】
(1)操作①能否改为“将加热后的表面有黑色氧化铜的铜丝插入盛有白酒的试管中”?不能,理由是乙酸也能使铜丝表面由黑色变为红色.
(2)K2Cr2O7中铬元素的化合价为+6.
白酒是乙醇的水溶液,酒中的乙醇在微生物作用下能被氧化成乙酸.小刚家有一瓶密封存放的白酒,他想知道该白酒的组成情况,于是进行如下实验探究:
【提出问题】该白酒中的溶质主要有哪些?
【查阅资料】
材料一:乙醇(C2H5OH),俗称酒精,易溶于水,水溶液呈中性.在加热条件下,可以把氧化铜还原为单质铜.
材料二:乙酸(CH3COOH),又名醋酸,易溶于水,具有酸的通性.
【提出猜想】
猜想1:只有乙醇
猜想2:只有乙酸
猜想3:乙醇和乙酸.
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量白酒于试管中,滴入几滴橙色的K2Cr2O7酸性溶液 | 溶液变成蓝绿色 | 猜想1成立 |
| ②取少量白酒于试管中,滴入几滴紫色石蕊试液 | 石蕊试液不变色 |
(1)操作①能否改为“将加热后的表面有黑色氧化铜的铜丝插入盛有白酒的试管中”?不能,理由是乙酸也能使铜丝表面由黑色变为红色.
(2)K2Cr2O7中铬元素的化合价为+6.
3.下列属于化学变化的是( )
| A. | 酒精的挥发 | B. | 金属锈蚀 | C. | 车胎爆炸 | D. | 石蜡受热熔化 |
20.下列有关实验操作的“先”和“后”的说法中,正确的是( )
| A. | 若不慎将腐蚀性药液溅入眼睛,要先用手揉眼睛,后用水冲洗 | |
| B. | 给试管里的药品加热时,先均匀加热,后集中加热 | |
| C. | 用滴管取细口瓶内的液体时,先将其伸入液体内,后挤压取液 | |
| D. | 向试管中装入固体粉末时,先将试管直立,后把盛药品的药匙送至试管底部 |