题目内容
2.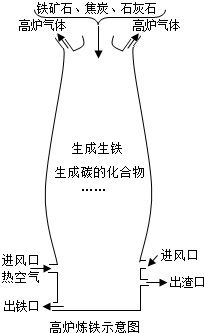 钢铁是使用最多的金属材料.
钢铁是使用最多的金属材料.(1)空气通过进风口与原料中的焦炭充分反应,其化学方程式为O2+C$\frac{\underline{\;点燃\;}}{\;}$CO2.
(2)由(1)中产生的气体与炽热的焦炭会继续反应,其化学方程式为CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
(3)生成铁的主要反应方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,该反应中发生氧化反应的物质是CO(填化学式).
(4)金属钴(CO)与铁具有相似的化学性质.COCl2固体是蓝色的,COCl2溶液是粉红色的.现将金属钴投入稀盐酸中,发生化学反应CO+2HCl=COCl2+H2↑.该反应的实验现象为金属不断溶解,表面产生气泡,溶液由无色变为粉红色.
分析 (1)根据碳完全燃烧的产物下化学方程式;
(2)根据二氧化碳与炽热碳的反应解答;
(3)在反应中,氧化铁失去了氧,发生了还原反应,是氧化剂.一氧化碳得到了氧,发生了氧化反应,是还原剂;
(4)根据物质的性质可以判断实验现象.
解答 解:(1)焦炭充分反应生成二氧化碳,化学方程式为O2+C$\frac{\underline{\;点燃\;}}{\;}$CO2;故填:O2+C$\frac{\underline{\;点燃\;}}{\;}$CO2;
(2)炼铁高炉内焦炭与二氧化碳反应生成一氧化碳,反应的化学方程式为:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;故填:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
(3)生成生铁的主要反应为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,由反应式可知,氧化铁在反应中失去了氧,发生了还原反应,是氧化剂,一氧化碳在反应中得到氧是还原剂;
故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;CO;
(4)金属钴投入稀盐酸中时,发生化学反应:Co+2HCl=CoCl2+H2↑,随着反应的进行,金属不断溶解,表面产生气泡,溶液由无色变为粉红色;故填:金属不断溶解,表面产生气泡,溶液由无色变为粉红色.
点评 此题是对炼铁知识的考查,解决的关键是知道炼铁的原理、原料及过程,属基础性知识考查题.

练习册系列答案
相关题目
14.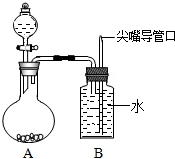 小明设计了趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加( )
小明设计了趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加( )
 小明设计了趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加( )
小明设计了趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加( )| A. | 氯化钠和水 | B. | 硝酸铵和水 | C. | 碳酸钙和稀盐酸 | D. | 铜和稀硫酸 |