题目内容
小东通过查阅资料.根据铁在空气中生锈的原理,设计了如图所示的实验装置来测定空气中氧气含量(装置中的饱和食盐水、活性炭会加速铁生 水锈)。已知产口瓶的有效容积为242mL ,实验8分钟后打开止水夹,水从烧杯流入广口瓶中的体积 浸有饱和食盐水为48ml。下列说法错误的是 
A. 该实验的不足之处在于实验前广口瓶底未放铁粉 ,活性炭粉少量水
B. 通过分析本次实验数据 ,可知空气中氧气的体积分数约为19. 8%
C. 若实验药品充足,时间足够长,可十分接近拉瓦锡实验的结果
D. 此实验可有效解决拉瓦锡实验中的汞污染问题
 阅读快车系列答案
阅读快车系列答案小雨阅读课外资料得知:氯酸钾的分解可用二氧化锰、氧化铜等物质作催化剂。于是,他对影响氯酸钾分解的因素及催化剂的催化效果产生了探究兴趣。
(提出问题)氧化铜是否比二氧化锰催化效果更好?影响氯酸钾分解速率的因素有哪些 呢?
(设计实验1小雨以生成等体积的氧气为标准,设计了下列几组实验。
序号 | KClO3的质量 | 其他物质的质量 | 温度 | 氧气的体积 | 反应所需时间 |
① | 10.0 g | 330℃ | 100 mL | t1 | |
② | 10.0 g | CuO 1.5 g | 330℃ | 100 mL | t2 |
③ | 10.0 g | MnO2 1.5 g | 330℃ | 100 mL | t3 |
④ | 10.0 g | MnO2 g | 380℃ | 100mL | t4 |
(1)若t1>t2,说明氧化铜能加快氯酸钾的分解速率。若要确定氧化铜是此反应的催化剂,还需探究反应前后,氧化铜的_________和_________不变。
(2)写出实验④所涉及的化学方程式__________________。
(3)实验④中MnO2的质量为_________g,若t3>t4,则化学反应快慢与温度的关系是_________。
(4)氯酸钾的分解速率可能还与_________因素有关,请设计实验证明_______。


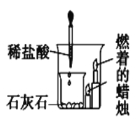 B.
B. 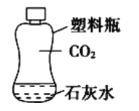
 D.
D.