题目内容
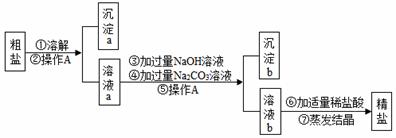 粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等).某班同学在粗盐提纯实验中,为把少量可溶性杂质CaCl2、MgCl2一并除去,将教材中实验方案修改设计如下,请据此回答问题:(1)实验操作A的名称是______。
粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等).某班同学在粗盐提纯实验中,为把少量可溶性杂质CaCl2、MgCl2一并除去,将教材中实验方案修改设计如下,请据此回答问题:(1)实验操作A的名称是______。
(2)写出步骤③中发生反应的主要化学方程式 ;
步骤⑥的作用是 。
(3)小刚同学认为实际得到的氯化钠可能比粗盐中含有的氯化钠要多,理由: 。
(1)过滤,除去难溶性杂质;
(2)MgCl2+2NaOH═Mg(OH)2↓+2NaCl, 除去过量的氢氧化钠和碳酸钠;
(3)因为在实验过程中有新的氯化钠生成.

练习册系列答案
相关题目
下列试剂能一次鉴别出稀硫酸、清石灰水、氢氧化钠溶液的是
|
| A. | 紫色石蕊试液 | B. | 酚酞试液 | C. | 碳酸钙粉末 | D. | 碳酸钾溶液 |
碱石灰是NaOH与CaO的混合物,取一定量露置于空气中部分变质的碱石灰,加水充分搅拌后过滤,所得物质成分可能是
| 选项 | A | B | C | D |
| 滤液中的溶质 | NaOH、Ca(OH)2 | NaOH | NaOH、Na2CO3 | Na2CO3 |
| 滤渣 | CaCO3、Ca(OH)2 | Ca(OH)2 | CaCO3、Ca(OH)2 | CaCO3 |
为了测定某纯碱样品(含少量氯化钠杂质)中碳酸钠的质量分数,取该样品与足量稀盐酸在烧杯中反应,有关实验数据如下表。
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的含量/g | 纯碱样品的质量/g | 烧杯及混合物的质量/g |
| 120 | 12 | 127.6 |
(1)反应生成二氧化碳的质量为______g。
(2)请计算:该纯碱样品中碳酸钠的质量分数为多少。
 于化学变化的是
于化学变化的是
 A~F是六种常见物质:铁、氧化钙、盐酸、氢氧化钙、硫酸铜、碳酸氢铵中的某一种,B是胃液中的主要成分,E常用于改良酸性土壤。他们之间的相互关系如右图所示(其中实线表示物质间可以相互反应,虚线表示物质间不直接能反应)。请回答下列问题:
A~F是六种常见物质:铁、氧化钙、盐酸、氢氧化钙、硫酸铜、碳酸氢铵中的某一种,B是胃液中的主要成分,E常用于改良酸性土壤。他们之间的相互关系如右图所示(其中实线表示物质间可以相互反应,虚线表示物质间不直接能反应)。请回答下列问题: 与E反应的化学方程式为
与E反应的化学方程式为 : ,该反应的基本反应类型是 反应,也称 反应。
: ,该反应的基本反应类型是 反应,也称 反应。 。已知达菲的化学式为C16H31N2PO8
。已知达菲的化学式为C16H31N2PO8