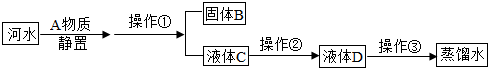
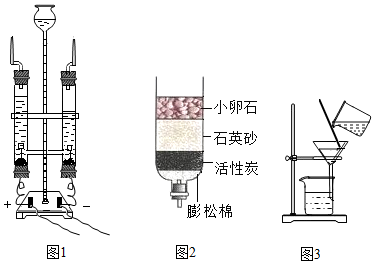
题目内容
17.下列各图是实验室用来制取气体的发生装置和收集装置,按下列要求填空.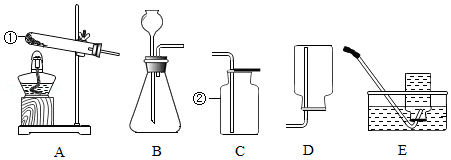
(1)写出图中仪器②的名称:集气瓶
(2)装置A 中试管口一定要略向下倾斜,其目的是防止冷凝水回流到热的试管底部,炸裂试管.
(3)实验室用高锰酸钾制取氧气并收集较纯净的氧气,所需的发生装置是A(填序号,以下同),收集装置是E,反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(4)用排水法收集氧气,收集氧气的最佳时间是导管口有连续均匀气泡产生时.
(5)实验结束时一定要先将导管从水槽中拿出,再熄灭酒精灯,其目的是防止水槽中的水倒吸回试管,使试管炸裂.
(6)已知在实验室可用稀盐酸(液体)和石灰石(固体)在常温下来制取二氧化碳气体,那么该反应所选取的发生装置为B(填序号)
分析 (1)根据常见仪器的名称与用途进行分析;
(2)根据给固体药品加热时的注意事项进行分析;
(3)发生装置的选择要看反应物的状态和反应条件;收集装置的选择要看气体的密度和溶解性;根据高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气写出化学方程式即可;
(4)根据用排水法开始收集氧气的适宜时刻是:导管口有连续均匀气泡产生时进行分析;
(5)根据实验室里用加热高锰酸钾的方法制取氧气的步骤及注意的事项分析;
(6)根据应物状态和反应条件选择发生装置即可.
解答 解:(1)图中②是集气瓶.
(2)给固体药品加热时,试管口一定要略向下倾斜,以防冷凝水回流到热的试管底部,炸裂试管;
(3)高锰酸钾制取氧气为固体加热型,发生装置选择A;氧气的密度比空气大,不易溶于水,因此可用排水法和向上排空气法受,但排水法收集的氧气更纯净;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(4)用排水法开始收集氧气的适宜时刻是:导管口有连续均匀气泡产生时;
(5)实验完毕,先把导气管移出水面,然后再熄灭酒精灯其原因是:防止水槽的水倒流回试管使试管炸裂;
(6)在常温下,用块状石灰石固体和稀盐酸制取二氧化碳气体,属于固液常温型,故选发生装置B;
故答案为:(1)集气瓶;(2)防止冷凝水回流到热的试管底部,炸裂试管;(3)A;E;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;(4)导管口有连续均匀气泡产生时;(5)防止水槽中的水倒吸回试管,使试管炸裂;(6)B;
点评 本题考查了常见气体发生装置和收集装置的选择,完成此题,可以依据已有的知识进行.要求同学们在完成此类题目时,要熟知反应物的状态和反应的条件以及气体的密度和水溶性,以便做出正确的判断.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 按质量计算,空气中含氮气78%,氧气21%,其他气体和杂质1% | |
| B. | 鱼类能在水中生活,证明氧气易溶于水 | |
| C. | 洁净的空气中纯净物,被污染的空气是混合物 | |
| D. | 实验室常用排水法收集氧气 |
| A. | 一氧化碳燃烧时,发出蓝色火焰 | |
| B. | 煤气中毒的实质是一氧化碳中毒 | |
| C. | 将二氧化碳通入紫色石蕊溶液,溶液变蓝 | |
| D. | 向种植蔬菜的大棚中补充二氧化碳有利蔬菜生长 |
| A. | 氢原子和氧原子在点燃条件下生成水分子 | |
| B. | 2份质量的氢气和1份质量的氧气在点燃的条件下生成2份质量的水 | |
| C. | 氢气与氧气在点燃的条件下反应生成水 | |
| D. | 氢元素和氧元素在点燃条件下生成水元素 |
| 选项 | 生活现象 | 分子的特性 |
| A | 篮球充气 | 分子间有一定的间隔 |
| B | 在花园里可闻到花的香味 | 分子在不断地运动 |
| C | 电解水可以得到氢气和氧气 | 化学反应时,分子可分 |
| D | 湿衣服晾干 | 分子的质量很小 |
| A. | A | B. | B | C. | C | D. | D |