题目内容
4.某反应的微观示意图按图所示.在一定条件下,将一定质量的A与18gB充分反应,当B反应完全时,生成14.5gC和6.5gD.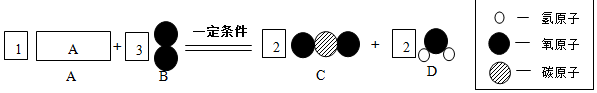
①
 的化学式为H2O.
的化学式为H2O.②参加反应A的质量是3g.
③组成A分子的原子是碳原子和氢原子.
④A分子中各元素的质量比是6:1.
⑤该反应中A、C两种物质的质量比为13:44.
⑥该反应的化学方程式是C2H4+3O2$\frac{\underline{\;一定条件\;}}{\;}$2CO2+2H2O.
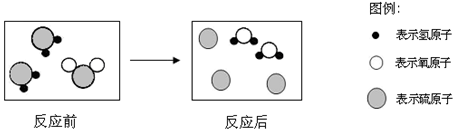
分析 根据反应的微观模拟示意图确定反应物A以及反应的化学方程式,在微观结构示意图中,由不同种原子构成的纯净物属于化合物,根据化学式的意义解答即可.
解答 解:①由图示可知: 的化学式为H2O;
的化学式为H2O;
②在化学反应前后,反应前各物质的质量总和等于反应后生成的各物质的质量总和,故A物质的质量为:14.5g+6.5g-18g=3g,故填:3g.
③根据质量守恒定律,化学反应前后原子的种类和数目不变,组成A分子的原子是碳原子和氢原子;
④根据质量守恒定律,化学反应前后原子的种类和数目不变,反应前C、H、O的原子个数分别是:0、0、6,反应后C、H、O的原子个数分别是:2、4、6;则1个A分子中有2各碳原子和4个氢原子,A的化学式为:C2H4,A分子中各元素的质量比是(12×2):(1×4)=6:1;
⑤根据图示可以看出,反应的物质是A、氧气,生成的物质是二氧化碳和水,该反应的化学方程式为C2H4+3O2$\frac{\underline{\;一定条件\;}}{\;}$2CO2+2H2O;
该反应中A、C两种物质的质量比为:(12×2+1×4):[2(12+16×2)]=13:44;
⑥该反应的化学方程式为:C2H4+3O2$\frac{\underline{\;一定条件\;}}{\;}$2CO2+2H2O;
故答案为:
①H2O;②3g;③碳原子和氢原子;④6:1;⑤13:44;⑥C2H4+3O2$\frac{\underline{\;一定条件\;}}{\;}$2CO2+2H2O.
点评 本题考查的是质量守恒定律的应用以及化学反应的微观模拟示意图的知识,完成此题,可以依据已有的知识结合图示进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列叙述、对应的化学方程式、所属基本反应类型都正确的是( )
| A. | 服用含氢氧化铝的药物治疗胃酸过多 Al(OH)3+3HCl═AlCl3+3H2O复分解反应 | |
| B. | 拉瓦锡研究空气成分 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2 分解反应 | |
| C. | 用天然气作燃料 CH4+O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 氧化反应 | |
| D. | 验证铜和铝的活动性 3Cu+Al2(SO4)3═3CuSO4+2Al 置换反应 |
 某补钙药剂的标签主要内容如图所示,现测定该钙片含量是否符合标注,做如下实验:取10片该钙片,放入干燥、洁净的烧杯中,再向烧杯中加入50g稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的质量为64.5g.
某补钙药剂的标签主要内容如图所示,现测定该钙片含量是否符合标注,做如下实验:取10片该钙片,放入干燥、洁净的烧杯中,再向烧杯中加入50g稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的质量为64.5g. 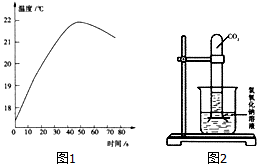 小组同学在学完中和反应知识后思考,除了通过酚酞变色说明氧氧化钠与稀盐酸能发生反应,还有什么方法能说明两者发生了反应?同学们讨论后进行以下实验探究.
小组同学在学完中和反应知识后思考,除了通过酚酞变色说明氧氧化钠与稀盐酸能发生反应,还有什么方法能说明两者发生了反应?同学们讨论后进行以下实验探究.