题目内容
实验室常用下列装置来制取氧气: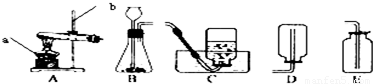
(1)写出图中有标号仪器的名称:a______、b______;
(2)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是______(填序号),请你写出发生反应的化学方程式______ 2H2O+O2↑
【答案】分析:(1)熟记常见仪器的名称;(2)根据反应物的状态确定发生装置,根据方程式的写法写出反应原理,根据催化剂所起的作用考虑二氧化锰的作用,根据氧气的性质和密度考虑收集方法和验满方法;(3)①根据质量守恒定律考虑化学式写法;②根据发生装置和收集装置的选取方法考虑;(4)根据物质的量、质量、摩尔质量的关系解答本题.
解答:解;(1)熟记常见仪器的名称和用途;
(2)双氧水是液体,二氧化锰是固体所以不需要加热;写方程式要注意一写二配三注明四等号.用过氧化氢制氧气时,反应物是过氧化氢,生成物是水和氧气,配平方法是用观察法配平,反应条件是二氧化锰作催化剂,氧气后面标上上升符号;二氧化锰是催化剂,催化剂所起的作用叫做催化作用;由于氧气密度比空气大所以用向上排空气法收集,由于氧气具有助燃性,能使带火星的木条复燃,所以验满方法是将带火星的木条放到集气瓶口,复燃说明满了;
(3)①根据反应前后各原子个数是不变的,由方程式可知生成物中缺少4个氢,2个氧,因为X的前面系数是2所以X的化学式为:H2O;
②制取NH3的反应条件需要加热,所以选择有酒精灯的装置;由于氨气易溶于水,不能用排水法收集,密度比空气小用向下排空气法收集;
(4)氯酸钾制取氧气的反应物是氯酸钾,生成物是氯化钾和氧气,用最小公倍数法配平即可,反应条件是二氧化锰作催化剂加热,氧气后面标上上升符号;①产生的氧气的质量是0.075mol×32g/mol=2.4g;②设分解的氯酸钾物质的量为X则:
2KClO3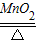 2KCl+3O2↑
2KCl+3O2↑
2 3
X 0.075mol
根据: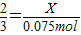 解得X=0.05mol.
解得X=0.05mol.
故答案为:(1)酒精灯;长颈漏斗;(2)B;2H2O2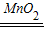 2H2O+O2↑;催化作用;氧气的密度比空气大;将带火星的木条放到集气瓶口,复燃说明满了;(3)①H2O;②A;D;(4)2KClO3
2H2O+O2↑;催化作用;氧气的密度比空气大;将带火星的木条放到集气瓶口,复燃说明满了;(3)①H2O;②A;D;(4)2KClO3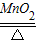 2KCl+3O2↑;2.4;0.05.
2KCl+3O2↑;2.4;0.05.
点评:通过回答本题识记了常见仪器的名称,熟悉了制取氧气的反应原理,氧气的验满方法,知道了发生装置和收集装置的选取方法,了解了物质的质量、物质量、摩尔质量三者的关系.
解答:解;(1)熟记常见仪器的名称和用途;
(2)双氧水是液体,二氧化锰是固体所以不需要加热;写方程式要注意一写二配三注明四等号.用过氧化氢制氧气时,反应物是过氧化氢,生成物是水和氧气,配平方法是用观察法配平,反应条件是二氧化锰作催化剂,氧气后面标上上升符号;二氧化锰是催化剂,催化剂所起的作用叫做催化作用;由于氧气密度比空气大所以用向上排空气法收集,由于氧气具有助燃性,能使带火星的木条复燃,所以验满方法是将带火星的木条放到集气瓶口,复燃说明满了;
(3)①根据反应前后各原子个数是不变的,由方程式可知生成物中缺少4个氢,2个氧,因为X的前面系数是2所以X的化学式为:H2O;
②制取NH3的反应条件需要加热,所以选择有酒精灯的装置;由于氨气易溶于水,不能用排水法收集,密度比空气小用向下排空气法收集;
(4)氯酸钾制取氧气的反应物是氯酸钾,生成物是氯化钾和氧气,用最小公倍数法配平即可,反应条件是二氧化锰作催化剂加热,氧气后面标上上升符号;①产生的氧气的质量是0.075mol×32g/mol=2.4g;②设分解的氯酸钾物质的量为X则:
2KClO3
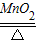 2KCl+3O2↑
2KCl+3O2↑2 3
X 0.075mol
根据:
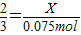 解得X=0.05mol.
解得X=0.05mol.故答案为:(1)酒精灯;长颈漏斗;(2)B;2H2O2
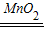 2H2O+O2↑;催化作用;氧气的密度比空气大;将带火星的木条放到集气瓶口,复燃说明满了;(3)①H2O;②A;D;(4)2KClO3
2H2O+O2↑;催化作用;氧气的密度比空气大;将带火星的木条放到集气瓶口,复燃说明满了;(3)①H2O;②A;D;(4)2KClO3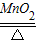 2KCl+3O2↑;2.4;0.05.
2KCl+3O2↑;2.4;0.05.点评:通过回答本题识记了常见仪器的名称,熟悉了制取氧气的反应原理,氧气的验满方法,知道了发生装置和收集装置的选取方法,了解了物质的质量、物质量、摩尔质量三者的关系.

练习册系列答案
相关题目

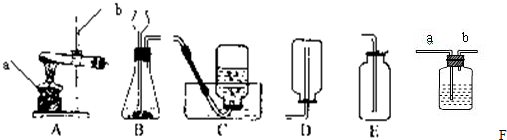

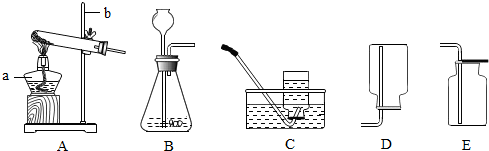
 实验室常用下列装置来制取氧气:
实验室常用下列装置来制取氧气: