题目内容
铜元素有多种氧化物,如CuO、Cu2O.称取14.4g仅含Cu、O两种元素的固体样品、采用如下装置实验(夹持装置省略)。测得实验前后装置B增重4.4g。下列说法正确的是( )

A. 装置B的作用是吸收反应生成的H2O和CO2
B. 实验开始前应先关闭K2,打开K1,让CO通一段时间
C. 根据实验数据进行计算,可以确定该固体为Cu2O
D. 若缺少装置C,则实验所得Cu、O个数比偏高
B 【解析】 A、装置A中的反应是CuO+COCu+CO2,Cu2O+CO2Cu+CO2,反应中没有生成水,装置B的作用是吸收反应生成的CO2,错误;B、一氧化碳是具有可燃性的气体,实验开始前应先关闭K2,打开K1,让CO通一段时间,排尽玻璃管中空气,防止加热时发生爆炸,正确。C、由题意可知装置B增重4.4g,是吸收二氧化碳的质量,由质量守恒定律可知,铜的氧化物中氧元素的质量是:4.4... 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案除去下列物质中混有的少量杂质所选用的操作方法,正确的是
选项 | 物质 | 操作方法 |
A | CO2混有HCl气体 | 将气体通过足量NaOH溶液 |
B | CuO混有碳粉 | 加入适量稀HCl,过滤、洗涤、干燥 |
C | NaCl溶液混有CaCl2 | 加入过量Na2CO3溶液、过滤 |
D | Cu(NO3)2溶液混有CuCl2 | 加入适量AgNO3溶液、过滤 |
A. A B. B C. C D. D
D 【解析】 A、二氧化碳与氯化氢气体都可以与氢氧化钠反应,故不能用氢氧化钠除去二氧化碳中的氯化氢,错误; B、氧化铜可以与稀盐酸反应,而碳不能与稀盐酸反应,故不能除去杂质,反而消耗了氧化铜,故错误; C、加入过量Na2CO3溶液后可以除去氯化钙,但是引入了碳酸钠杂质,故错误; D、Cu(NO3)2溶液混有CuCl2加入适量AgNO3溶液可以除去氯化铜,且不生成其他杂...某化学学习小组的同学对一瓶敞口放置氢氧化钙固体的化学成分产生了兴趣,他们根据自己所学知识进行如下探究:
[提出问题]该瓶药品的化学成分是什么?
[查阅资料](1)氢氧化钙能与空气中的二氧化碳反应而变质。
(2)氢氧化钙的溶解度曲线如图:
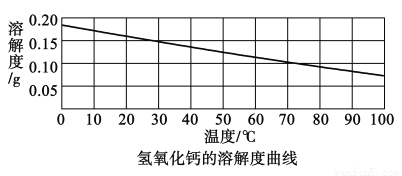
[猜想假设]猜想一:Ca(OH)2
猜想二:__________
猜想三:CaCO3
[实验验证]
实验操作 | 实验现象 | 实验结论 |
(1)取1g样品放入盛有50g水的烧杯中,充分搅拌后,静置 | 烧杯底部有较多固体未溶解 | 样品中含有CaCO3 |
(2)取实验(1)中上层清液少许于试管中,再向试管中滴加2~3滴无色酚酞试液 | _____________ | 样品中含有Ca(OH)2 |
[得出结论]甲同学认为猜想二正确。
[反思交流]
(1)乙同学认为甲同学的结论不合理,他认为猜想_____也可能正确,原因是______。
(2)丙同学认为要想验证猜想二正确,还需做如下实验:取实验(1)中未溶解固体于试管中,向试管中滴加适量稀盐酸,如有_______,则猜想二正确。
[拓展提升]要想验证反应后物质的成分,除需验证有生成物以外,还应考虑反应物是否________________。
Ca(OH)2和CaCO3 溶液由无色变成红色 一 氢氧化钙微溶于水,未溶解固体可能只含氢氧化钙 气泡产生. 有剩余 【解析】本题通过氢氧化钙变质探究实验考查了碱的性质,碳酸根离子的检验等。解答时要根据各种物质的性质,结合各方面条件进行分析、判断得出正确的结论。 猜想假设:氢氧化钙能与空气中的二氧化碳生成碳酸钙和水。若没有变质,则固体成分是Ca(OH)2,部分变质固体成分是Ca(O...





