题目内容
1.我们用如图测定空气中氧气的含量,回答下列问题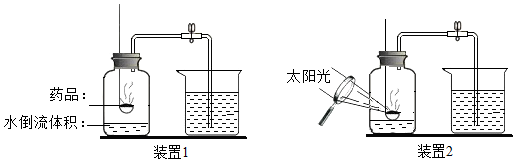
(1)装置1该实验可看到的现象:发黄光、冒白烟、放出热量,烧杯中的水进入集气瓶,约占集气瓶容积的五分之一.
(2)该实验的结论:氧气约占空气体积的五分之一.
(3)该实验还可以说明剩下的主要气体氮气有那些性质?
不能支持燃烧.
(4)反应的符号表达式:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(5)如果该实验测得的氧气的体积少于五分之一,可能的原因有:①红磷的量不足;②装置漏气.
(6)与装置1相比,装置2有什么优点减小了误差,避免了P2O5对空气的污染.
分析 (1)根据红磷燃烧的现象以及空气中的氧气的含量来分析;
(2)根据进入集气瓶的水的体积来分析;
(3)从实验现象分析氮气的性质去分析解答;
(4)根据反应的原理以及化学方程式的写法来分析;
(5)根据实验的注意事项来分析解答;
(6)根据实验的改进来分析.
解答 解:(1)红磷燃烧发出黄光、冒出白烟、放出热量;当装置冷却至室温后,打开止水夹,发现烧杯中的水进入集气瓶,进入的水的体积约占集气瓶容积的五分之一;故填:发黄光、冒白烟、放出热量,烧杯中的水进入集气瓶,约占集气瓶容积的五分之一;
(2)进入的水的体积即为集气瓶内的氧气气体,由实验后的现象可知,氧气约占空气体积的五分之一;故填:氧气约占空气体积的五分之一;
(3)由冷却,打开止水夹,烧杯中的水倒流进试管中,液面上升到一定高度不再上升.说明了氮气的溶解性是难溶于水,由红磷不能与氮气反应,说明了氮气的性质不活泼等.故填:不能支持燃烧(答案合理即可);
(4)磷与氧气在点燃的条件下反应生成五氧化二磷;故填:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(5)某同学做该实验时,测出氧气的含量远远低于实际值,请你分析其中的原因:①红磷不足量;②装置的气密性不好;③未冷却至室温就打开止水夹等.故填:红磷的量不足;装置漏气;
(6)改进后的实验在密闭环境中进行,减小了误差,避免了P2O5对空气的污染;故填:减小了误差,避免了P2O5对空气的污染.
点评 本题主要考查用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,难度稍大.

练习册系列答案
相关题目
11.有关碳和碳的化合物描述错误的是( )
| A. | 干冰常用于人工降雨 | |
| B. | 活性炭具有较强的吸附性,常用于工业制白糖时脱色 | |
| C. | 金刚石和石墨由于碳原子排列方式不同,物理性质不同 | |
| D. | 室内放一盆水可以防止一氧化碳中毒 |
12. 某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示.下列说法正确的是( )
某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示.下列说法正确的是( )
 某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示.下列说法正确的是( )
某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象,如图所示.下列说法正确的是( )| A. | 图中c点所示溶液呈碱性 | |
| B. | 图中a点所示溶液中,含有的溶质是Na2SO4和H2SO4 | |
| C. | 由a点到b点的pH变化过程证明酸和碱发生了中和反应 | |
| D. | 该实验是将氢氧化钠溶液逐滴滴入到盛有硫酸的烧杯中 |
9.国际互联网上报道:“目前世界上有近20亿人患有缺铁性贫血”.我国政府将启动“酱油补铁工程”.这里的铁是指( )
| A. | 铁单质 | B. | 四氧化三铁 | C. | 三氧化二铁 | D. | 铁元素 |
16.空调和冰箱中的制冷剂“氟里昂”(以M代表其化学式),逸散到大气中可和臭氧发生反应,其反应过程可简示为:M+O3→MO+O2,MO+O→M+O2.据此判断哪种物质最有可能是该反应过程的催化剂( )
| A. | M | B. | O3 | C. | O2 | D. | MO |
13.下列实验现象描述正确的是( )
| A. | 蜡烛在空气中燃烧发出淡蓝色火焰 | |
| B. | 铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 | |
| C. | 木炭在氧气中燃烧生成二氧化碳 | |
| D. | 硫磺在氧气中燃烧发出蓝紫色火焰,产生有刺激性气味的气体 |
10.下列反应属于分解反应的是( )
| A. | 石蜡在空气中燃烧 | B. | 硫在氧气中燃烧 | ||
| C. | 电解水生成氢气和氧气 | D. | 加热汞变成氧化汞 |
11.用量筒量取溶液,仰视凹液面最低处,读数为17mL,倒出部分液体后,俯视凹液面的最低处,读数为7mL,则该学生实际倒出的溶液体积( )
| A. | 大于10mL | B. | 小于10mL | C. | 等于10mL | D. | 无法确定 |
