题目内容
8.画出下列微粒的结构示意图.(1)氧原子
 (2)氧离子
(2)氧离子 (3)氮原子
(3)氮原子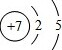
(4)硫原子
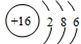 (5)氯离子
(5)氯离子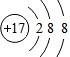 (6)铝离子
(6)铝离子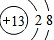 .
.
分析 根据原子结构示意图和离子结构示意图的画法来分析解答.
解答 解:(1)氧原子的核内质子数为8,核外电子数为8,故答案为: ;
;
(2)氧原子最外层有6个电子,易得到2个使得最外层达到8个电子的稳定结构,故填: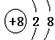 ;
;
(3)氮原子核内质子数为7,核外电子数为7,故填: ;
;
(4)硫原子核内有16个质子,核外有16个电子,故填: ;
;
(5)氯离子是由氯原子得到1个电子而形成的,核内质子数为17,核外电子数为18,故填: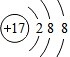 ;
;
(6)铝原子核内有13个质子,核外有13个电子,最外层有3个电子,易失去最外层的3个电子,使得次外层变成最外层而达到8个电子的稳定结构;故填: .
.
点评 了解原子结构示意图与离子结构示意图的区别和联系;掌握原子和离子的相互转化的特点.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
13.以下是四位同学净化水的操作,其中正确的是( )
| A. | 王蒙:静置沉淀→蒸馏→过滤→吸附沉淀 | |
| B. | 张凯:静置沉淀→过滤→吸附沉淀→蒸馏 | |
| C. | 秦乐:静置沉淀→吸附沉淀→过滤→蒸馏 | |
| D. | 郭晓:吸附沉淀→静置沉淀→蒸馏→过滤 |
3. 化学知识学习过程也是学习方法的积累过程.
化学知识学习过程也是学习方法的积累过程.
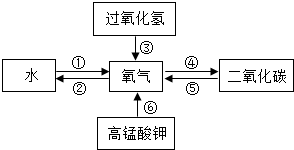
(1)构建知识网络是一种重要的学习方法,如图是某同学构建的有关氧气获得和性质的网络图,请根据题图回答有关问题:
【1】电解水是实现转化①的途径之一,请写出该反应的化学方程式:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
【2】实验室用③转化获得氧气的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
【3】二氧化碳和氧气相互转化的方法很多.在自然界中二氧化碳转化为氧气的主要途径是绿色植物的光合作用.
【4】利用氢气作清洁能源,是转化②的反应之一,写出该化学反应方程式2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
(2)比较、推理是化学学习常用的方法.以下是根据一些实验事实推理出的影响化学反应的因素,其中推理不合理的是D.
 化学知识学习过程也是学习方法的积累过程.
化学知识学习过程也是学习方法的积累过程.(1)构建知识网络是一种重要的学习方法,如图是某同学构建的有关氧气获得和性质的网络图,请根据题图回答有关问题:
【1】电解水是实现转化①的途径之一,请写出该反应的化学方程式:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
【2】实验室用③转化获得氧气的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
【3】二氧化碳和氧气相互转化的方法很多.在自然界中二氧化碳转化为氧气的主要途径是绿色植物的光合作用.
【4】利用氢气作清洁能源,是转化②的反应之一,写出该化学反应方程式2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
(2)比较、推理是化学学习常用的方法.以下是根据一些实验事实推理出的影响化学反应的因素,其中推理不合理的是D.
| 序号 | 实验事实 | 影响化学反应的因素 |
| A | 铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧 | 反应物浓度 |
| B | 碳在常温下不与氧气发生反应,而在点燃时能与氧气反应 | 反应温度 |
| C | 双氧水在常温下缓慢分解,而在加入二氧化锰后迅速分解 | 有、无催化剂 |
| D | 铜片在空气中很难燃烧,铜粉在空气中较易燃烧 | 反应物的种类 |
13.下列选项没有错误的是( )
| A | 液态氧--火箭的燃料 | B | 决定元素的种类--质子数 |
| 人体中含量最多的元素-氧 | 决定元素的化学性质--最外层电子数 | ||
| C | 铁--由分子构成 | D | 分子--化学变化中的最小粒子 |
| 二氧化碳--由原子构成 | 原子--保持物质化学性质的最小粒子 |
| A. | A | B. | B | C. | C | D. | D |
17.某同学梳理并归纳了以下知识点:
①质子数相同的两种粒子不一定属于同种元素;
②某物质中只含一种元素,则该物质一定是纯净物;
③空气中氧气约占空气质量的21%;
④最外层电子数为8的粒子不一定是稀有气体元素的原子;
⑤由同种分子构成的物质一定是纯净物,但纯净物不一定是由同种分子构成的;
⑥原子是构成物质的最小粒子.其中正确的是( )
①质子数相同的两种粒子不一定属于同种元素;
②某物质中只含一种元素,则该物质一定是纯净物;
③空气中氧气约占空气质量的21%;
④最外层电子数为8的粒子不一定是稀有气体元素的原子;
⑤由同种分子构成的物质一定是纯净物,但纯净物不一定是由同种分子构成的;
⑥原子是构成物质的最小粒子.其中正确的是( )
| A. | ①②④ | B. | ①④⑤ | C. | ①③⑥ | D. | ②④⑤ |
18.二硫化碳(化学式为CS2)是一种易挥发、易燃、有毒、难溶于水的液体.下列有关说法不正确的是( )
| A. | 二硫化碳是由碳元素和硫元素组成的化合物 | |
| B. | 每个二硫化碳分子里含有2个硫原子 | |
| C. | 二硫化碳的化学性质很稳定,很难发生化学反应 | |
| D. | 二硫化碳是易燃、有毒的化学试剂,应该密封保存 |