题目内容
实验室制取氧气时,某同学取定量的高锰酸钾加热,记录产生氧气的质量与反应时间的关系如图1所示,请回答下列问题:
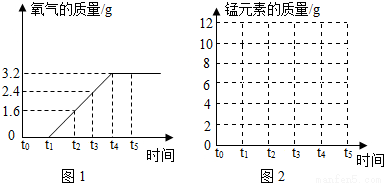
(1)t0﹣t1和t4﹣t5时段固体质量都不变,为什么?
(2)请根据图中数据计算高锰酸钾的质量为多少?(写出计算过程)
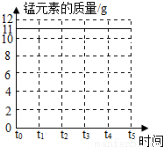
(3)请在图2坐标中,画出固体中锰元素质量在t0﹣t5时段变化示意图.
1.(1)t0-t1固体质量不变,是因为反应还未进行;(1分)t4-t5时固体质量不变,是因为反应进行完全;(1分)
(2)设高锰酸钾的质量是x
2KMnO4 K2MnO4+MnO2+O2↑(1分)
K2MnO4+MnO2+O2↑(1分)
316 32
x 3.2g
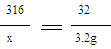
x=31.6g (1分)
答:高锰酸钾的质量为31.6g
(3)见图。
【解析】
试题分析:(1)t0-t1固体质量不变,是因为高锰酸钾还未进行反应,;t4-t5时固体质量不变,是因为高锰酸钾已经完全反应,无剩余。(2)根据图示知,高锰酸钾完全反应,产生氧气的质量为3.2克,利用化学方程式进行计算即可。(3)根据质量守恒定律可知,高锰酸钾完全分解产生氧气,生成固体为二氧化锰和锰酸钾,所以锰元素在化学反应中质量保持不变。
考点:图像与化学方程式相结合的计算题。

练习册系列答案
相关题目
 ,后集中加热。
,后集中加热。
 Na2SiO3 + X + H2O,下列有关X物质的化学式推断中,正确的是
Na2SiO3 + X + H2O,下列有关X物质的化学式推断中,正确的是
 持燃烧,说明氧气具有可燃性
持燃烧,说明氧气具有可燃性