题目内容
18.盐和碱是两类重要的物质,它们之间发生的反应是中学化学中重要的学习内容,在日常生活和工农业生产中也有广泛的应用.向一盛有硫酸钠的烧杯中逐滴加入氢氧化钡溶液,在这过程中发生的反应的化学方程式为Ba(OH)2+Na2SO4=2NaOH+BaSO4↓,随着氢氧化钡溶液的滴 入,烧杯溶液中减少的离子是硫酸根离子,增加的离子是氢氧根离子.从开始滴入氢氧化钡溶液直至过量,生成沉淀的质量与加入氢氧化钡溶液的质量关系正确的图象是A.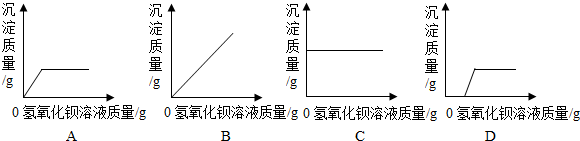
分析 根据硫酸钠与氢氧化钡反应生成了硫酸钡沉淀和氢氧化钠分析回答有关的问题.
解答 解:向一盛有硫酸钠的烧杯中逐滴加入氢氧化钡溶液生成了硫酸钡沉淀和氢氧化钠,在这过程中发生的反应的化学方程式为:Ba(OH)2+Na2SO4=2NaOH+BaSO4↓,随着氢氧化钡溶液的滴入,烧杯溶液中减少的离子是硫酸根离子,增加的离子是氢氧根离子.从开始滴入氢氧化钡溶液直至过量,生成沉淀的质量逐渐增加,当硫酸钠完全反应时不再增加,所以生成沉淀的质量与加入氢氧化钡溶液的质量关系正确的图象是A.
故答为:Ba(OH)2+Na2SO4=2NaOH+BaSO4↓,硫酸根离子,氢氧根离子,A.
点评 本题的难度不大,了解硫酸钠与氢氧化钡反应的实质是解答本题的基础.

练习册系列答案
相关题目
7.下列关于催化剂的说法中,正确的是( )
| A. | 只有二氧化锰能做催化剂 | |
| B. | 催化剂加快反应速率 | |
| C. | 催化剂不能减缓反应速率 | |
| D. | 反应前后催化剂的化学性质不会改变 |
8.酸、碱、盐是几类重要的化合物,他们之间能发生复分解反应.
(1)复分解反应发生的条件是有沉淀析出,或有气体放出,或有水生成.
(2)某化学小组进行“酸和碱的中和反应”实验:将盐酸滴入一定量的澄清石灰水中,实验无明显现象.取反应后的部分溶液加热、蒸干、得到白色固体.
以下是探究白色固体成分的实验,已知CaCl2溶液呈中性.请填写下表:
实验反思:无明显现象的中和反应可借助酸碱指示剂判断反应终点.
(3)“粗盐提纯”指除去NaCl中的泥沙和MgCl2、CaCl2、Na2SO4等杂质.
某同学设计了除去三种可溶性杂质的实验方案:先将固体溶解,然后向其中依次加入过量的BaCl2、NaOH、Na2CO3溶液,充分反应后过滤,蒸发结晶.请回答:
①溶解、过滤和蒸发操作中都用到一种玻璃仪器,该仪器在蒸发操作中的作用是什么?
②加入Na2CO3溶液的目的是什么?
③以上方案还需完善,请说明原因并加以补充.
(4)工业上常用NaOH溶液处理铝土矿(主要成分为A12O3),反应的化学方程式为:Al2O3+2NaOH=2NaAlO2+H2O(杂质不参与反应也不溶于水).若用160kg NaOH配制的溶液恰好能处理340kg铝土矿,最终得到1004kg NaAlO2溶液.
计算①该铝土矿中A12O3的质量分数.
②加入的NaOH溶液中水的质量.
(1)复分解反应发生的条件是有沉淀析出,或有气体放出,或有水生成.
(2)某化学小组进行“酸和碱的中和反应”实验:将盐酸滴入一定量的澄清石灰水中,实验无明显现象.取反应后的部分溶液加热、蒸干、得到白色固体.
以下是探究白色固体成分的实验,已知CaCl2溶液呈中性.请填写下表:
| 实验操作 | 测定结果 | 白色固体成分 |
| 用pH试纸测定反应后溶液的酸碱度,操作方法是 | pH>7 | |
| CaCl2 |
(3)“粗盐提纯”指除去NaCl中的泥沙和MgCl2、CaCl2、Na2SO4等杂质.
某同学设计了除去三种可溶性杂质的实验方案:先将固体溶解,然后向其中依次加入过量的BaCl2、NaOH、Na2CO3溶液,充分反应后过滤,蒸发结晶.请回答:
①溶解、过滤和蒸发操作中都用到一种玻璃仪器,该仪器在蒸发操作中的作用是什么?
②加入Na2CO3溶液的目的是什么?
③以上方案还需完善,请说明原因并加以补充.
(4)工业上常用NaOH溶液处理铝土矿(主要成分为A12O3),反应的化学方程式为:Al2O3+2NaOH=2NaAlO2+H2O(杂质不参与反应也不溶于水).若用160kg NaOH配制的溶液恰好能处理340kg铝土矿,最终得到1004kg NaAlO2溶液.
计算①该铝土矿中A12O3的质量分数.
②加入的NaOH溶液中水的质量.


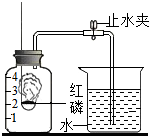 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下: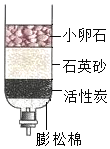 如图是某同学制作的简易净水器,请回答下列问题:
如图是某同学制作的简易净水器,请回答下列问题: