题目内容
1.现有Cu与另一种金属M(M可能是Mg、Fe、Zn中的一种)形成的粉末.现欲测定其组成,进行如下实验:取该粉末16g放入烧杯,将溶质质量分数为14%的稀硫酸280.0g分4次加入该烧杯中,充分反应后,测得剩余的固体质量数据记录如下:| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 70.0 | 70.0 | 70.0 | 70.0 |
| 剩余固体质量/g | 13.6 | 11.2 | 8.8 | 7.6 |
(1)该粉末中Cu的质量7.6g.
(2)该粉末中另一种金属M为何种金属?
(3)4次反应完全后过滤所得溶液的质量.
分析 铜不能和稀硫酸反应,镁、铁和锌与稀硫酸反应生成氢气和相应的盐,根据反应的化学方程式和提供的数据可以进行相关方面的判断和计算.
解答 解:(1)由表中数据可知,该粉末中Cu的质量是7.6g.
故填:7.6g.
(2)设金属的相对原子质量为x,
M+H2SO4=MSO4+H2↑,
x 98
2.4g 70g×14%
$\frac{x}{2.4g}$=$\frac{98}{70g×14%}$,
x=24,
答:镁的相对原子质量是24,因此该金属是镁.
(3)设4次反应后共生成氢气质量为y,
Mg+H2SO4=MgSO4+H2↑,
24 2
8.4g y
$\frac{24}{8.4g}$=$\frac{2}{y}$,
y=0.7g,
4次反应完全后过滤所得溶液的质量为:16g-7.6g+280g-0.7g=287.7g,
答:4次反应完全后过滤所得溶液的质量是287.7g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.工业用盐亚硝酸钠(NaNO2)有毒,其外观与食盐极为相似,其氮元素的化合价为( )
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
13.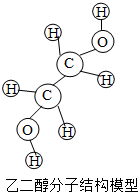 乙二醇(ethylene glycol)又名“甘醇”,分子结构如图结构模型.乙二醇是无色无臭、有甜味液体,对动物有毒性,人类致死剂量约为1.6g/kg.乙二醇能与水互溶,是合成涤纶的原料.下列有关乙二醇的叙述错误的是( )
乙二醇(ethylene glycol)又名“甘醇”,分子结构如图结构模型.乙二醇是无色无臭、有甜味液体,对动物有毒性,人类致死剂量约为1.6g/kg.乙二醇能与水互溶,是合成涤纶的原料.下列有关乙二醇的叙述错误的是( )
 乙二醇(ethylene glycol)又名“甘醇”,分子结构如图结构模型.乙二醇是无色无臭、有甜味液体,对动物有毒性,人类致死剂量约为1.6g/kg.乙二醇能与水互溶,是合成涤纶的原料.下列有关乙二醇的叙述错误的是( )
乙二醇(ethylene glycol)又名“甘醇”,分子结构如图结构模型.乙二醇是无色无臭、有甜味液体,对动物有毒性,人类致死剂量约为1.6g/kg.乙二醇能与水互溶,是合成涤纶的原料.下列有关乙二醇的叙述错误的是( )| A. | 乙二醇的化学式为C2H602 | |
| B. | 乙二醇分子是由碳、氢、氧三种元素组成的 | |
| C. | 每个乙二醇分子中含有34个电子 | |
| D. | 乙二醇中碳、氢、氧三种元素的质量比为12:3:16 |
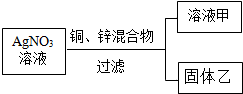 金属是重要的资源,在日常生活中已得到越来越广泛的应用,如图,向一定量AgNO3溶液中加入铜和锌的混合粉末,充分反应过滤,得溶液甲和固体乙.
金属是重要的资源,在日常生活中已得到越来越广泛的应用,如图,向一定量AgNO3溶液中加入铜和锌的混合粉末,充分反应过滤,得溶液甲和固体乙.
 某钙片的标签如图所示
某钙片的标签如图所示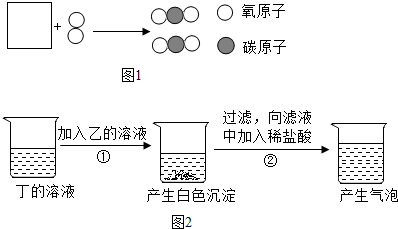
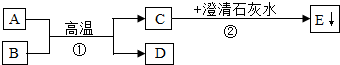 已知A、B为两种黑色粉末,D为红色单质.A、B、C、D、E五种物质之间的转化关系如图所示.
已知A、B为两种黑色粉末,D为红色单质.A、B、C、D、E五种物质之间的转化关系如图所示.