题目内容
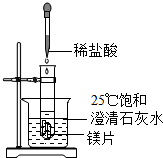 化学兴趣小组用如图装置进行实验,发现镁片完全溶解、石灰水浑浊.
化学兴趣小组用如图装置进行实验,发现镁片完全溶解、石灰水浑浊.(一)石灰水变浑浊的原因是:
(1)镁和盐酸的反应
(2)
(二)甲同学测得反应后试管内溶液pH<7
(1)该溶液呈
(2)该溶液pH<7的可能原因是:
①MgCl2溶液的pH<7; ②
(三)乙同学将反应后试管内溶液冷却,加入镁粉并滴入酚酞,溶液颜色无变化,再加热,发现溶液慢慢浑浊且变红.
【猜想】对实验中“溶液慢慢浑浊且变红”的原因,乙同学提出猜想:
MgCl2+2H2O=Mg(OH)2↓+2HCl,大家都认为此猜想不合理,理由是
【查阅】资料1:Mg(OH)2难溶解于水,升高温度可加大其在水中的溶解度.
资料2:K、Ca、Na、Mg等活泼金属在一定条件下能与水反应,产生碱和气体.
【实验】丙同学在滴有酚酞的热水中加入镁粉,观察到液体慢慢变红并浑浊,镁粉表面产生气泡.收集并点燃气体,发现能燃烧,该气体是
用化学方程式表示:乙同学实验中“溶液慢慢浑浊且变红”的原因
考点:物质发生化学变化时的能量变化,固体溶解度的影响因素,酸碱指示剂及其性质,溶液的酸碱性与pH值的关系,书写化学方程式、文字表达式、电离方程式
专题:综合实验题
分析:(一)镁与酸反应是一个放热反应,氢氧化钙的溶解度随温度的升高而减小;
(二)根据溶液酸碱性与酸碱度的关系以及酸可能过量来分析作答;
(三)【猜想】根据酸碱不能共存来分析;
【实验】根据反应过程和气体的性质来确定气体种类;镁能与热水反应生成氢氧化镁和氢气.
(二)根据溶液酸碱性与酸碱度的关系以及酸可能过量来分析作答;
(三)【猜想】根据酸碱不能共存来分析;
【实验】根据反应过程和气体的性质来确定气体种类;镁能与热水反应生成氢氧化镁和氢气.
解答:解:(一)氢氧化钙的溶解度随着温度的升高而减小,可见镁与稀盐酸反应是放热反应;
(二)pH<7,溶液显酸性,可能是氯化镁溶液显酸性,也可能是盐酸有剩余;
(三)【猜想】氢氧化镁是一种碱,不能与盐酸共存;
【实验】根据题干信息可知,该气体是镁与水反应生成的,且具有可燃性,所以是氢气;该反应是镁与水在加热的条件下反应生成氢氧化镁和氢气.
故答案为:(一)(1)放热;(2)Ca(OH)2的溶解度随温度升高而降低;
(二)(1)酸;(2)盐酸过量;
(三)Mg(OH)2能和HCl发生反应;H2;Mg+2H2O
Mg(OH)2↓+H2↑.
(二)pH<7,溶液显酸性,可能是氯化镁溶液显酸性,也可能是盐酸有剩余;
(三)【猜想】氢氧化镁是一种碱,不能与盐酸共存;
【实验】根据题干信息可知,该气体是镁与水反应生成的,且具有可燃性,所以是氢气;该反应是镁与水在加热的条件下反应生成氢氧化镁和氢气.
故答案为:(一)(1)放热;(2)Ca(OH)2的溶解度随温度升高而降低;
(二)(1)酸;(2)盐酸过量;
(三)Mg(OH)2能和HCl发生反应;H2;Mg+2H2O
| ||
点评:本题考查的知识点较多,难点是化学实验方案的设计与评价,学会运用猜想与事实验证的方法和技巧处理实验问题.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
“垃圾是放错了位置的资源”,应该分类回收.生活中废弃的铁锅、铝制易拉罐、铜导线等可以归为一类加以回收,它们属于( )
| A、氧化物 | B、非金属 |
| C、金属或合金 | D、碱 |
下列化学方程式符合题意,且书写正确的是( )
| A、比较铁和铜的活动性:Fe+Cu(OH)2═Cu+Fe(OH)2 |
| B、用熟石灰处理硫酸厂污水中的硫酸:H2SO4+Ca(OH)2═CaSO4+2H2O |
| C、用小苏打治疗胃酸过多症的反应:2NaHCO3+H2SO4═Na2SO4+CO2↑+2H2O |
| D、稀盐酸去除铁锈:6HCl+Fe2O3═2FeCl3+6H2O |
下列变化中,发生了化学变化的是( )
| A、钢铁生锈 | B、冰雪融化 |
| C、干冰升华 | D、矿石粉碎 |
 水是重要的自然资源,是人类赖以生存的物质基础.
水是重要的自然资源,是人类赖以生存的物质基础.