题目内容
4.科学施肥是实现农业增产的主要手段,硝酸铵(NH4NO3)是一种常用的化肥.(1)NH4NO3属于氮肥(填“钾肥”、“氮肥”或“复合肥料”)
(2)NH4NO3其中氮、氢、氧三种元素的质量比为7:1:12.NH4NO3的质量分数为35%.
(3)若要配制200g溶质质量分数为5%的硝酸铵溶液,需要硝酸铵的质量为10g,需要水的质量为190g.
分析 (1)根据化肥的种类分析即可;
(2)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答硝酸铵NH4NO3中氮元素、氢元素、氧元素的质量比;根据物质中某元素的质量分数=$\frac{该元素的相对原子质量×原子个数}{化合物的相对分子质量}$×100%,进行解答硝酸铵NH4NO3中氮元素的质量分数.
(3)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得蒸馏水的质量.
解答 解:(1)硝酸铵是氮肥;
(2)硝酸铵的相对分子质量:(14×2)+(4×1)+(16×3)=80,所以,硝酸铵中氮元素质量分数=$\frac{14×2}{80}$×100%=35%;
化合物中各元素质量比=各元素的相对原子质量×原子个数之比,因此硝酸铵(NH4NO3)中氮、氢、氧的质量比为:(14×2):(4×1):(16×3)=7:1:12;
(3)配制200g溶质质量分数为5%的硝酸铵溶液,需要硝酸铵的质量为200g×5%=10g;需要水的质量为为:200g-10g=190g.
故答案为:氮肥;7:1:12;35%;10;190.
点评 本题主要考查学生对物质中某元素的质量分数以及各元素质量比的计算,难度不大,但要注意计算的格式和结果的准确性.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
19.将一小块银白色的金属钠放置在空气中会发生下列变化:
钠(Na)$\stackrel{O_{2}}{→}$钠的氧化物$\stackrel{H_{2}O}{→}$氢氧化钠溶液$\stackrel{CO_{2}}{→}$白色固体
[提出问题]
常温下钠与氧气反应,产物有哪些?
[查阅资料]
钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠和过氧化钠都能与水发生反应,方程式如下:Na2O+H2O═2NaOH;2Na2O2+2H2O═4NaOH+O2↑
[作出猜想]
常温下钠与氧气反应的产物.
猜想1:Na2O;
猜想2:Na2O2;
猜想3:Na2O和Na2O2.
[实验探究一]
[继续探究]钠在空气中放置一段时间后得到的白色固体的成分.
[作出猜想]
猜想一:Na2CO3,
猜想二,Na2CO3和NaOH
[实验探究二]
[实验反思]
(1)类比氧化铜与盐酸的反应,写出氧化钠与盐酸反应的化学方程式Na2O+2HCl=2NaCl+H2O.
(2)过氧化钠也能与盐酸反应,方程式为2Na2O2+4HCl═4NaCl+2H2O+X↑,X的化学式为O2.
钠(Na)$\stackrel{O_{2}}{→}$钠的氧化物$\stackrel{H_{2}O}{→}$氢氧化钠溶液$\stackrel{CO_{2}}{→}$白色固体
[提出问题]
常温下钠与氧气反应,产物有哪些?
[查阅资料]
钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠和过氧化钠都能与水发生反应,方程式如下:Na2O+H2O═2NaOH;2Na2O2+2H2O═4NaOH+O2↑
[作出猜想]
常温下钠与氧气反应的产物.
猜想1:Na2O;
猜想2:Na2O2;
猜想3:Na2O和Na2O2.
[实验探究一]
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | 没有气泡生成 | 猜想1正确 |
[作出猜想]
猜想一:Na2CO3,
猜想二,Na2CO3和NaOH
[实验探究二]
| 实验操作 | 实验现象 | 实验结论 |
| 1.取少量白色固体加入足量氯化钙溶液 | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
| 2.过滤,取少量滤液加入无色的酚酞试液 | 变成红色 |
(1)类比氧化铜与盐酸的反应,写出氧化钠与盐酸反应的化学方程式Na2O+2HCl=2NaCl+H2O.
(2)过氧化钠也能与盐酸反应,方程式为2Na2O2+4HCl═4NaCl+2H2O+X↑,X的化学式为O2.
9.下列鉴别方法不可行的是( )
| A. | 用灼烧法鉴别羊毛线与棉纱线 | |
| B. | 用点燃的木条鉴别氯酸钾与氯化钾 | |
| C. | 用带火星的木条鉴别二氧化碳和氧气 | |
| D. | 用酚酞试液鉴别稀硫酸与氢氧化钠溶液 |
13. 红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
提出问题:久置固体的成分是什么?
查阅资料:铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
作出猜想:久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
久置固体中可能含有Ca(OH)2的原因是:
用化学方程式表示CaO+H2O=Ca(OH)2.
实验探究1:甲同学的方案(见表).
实验质疑:
(1)乙同学认为甲同学的实验中的实验中不能得出一定含有Ca(OH)2的结论,理由是因为CaO会与水反应生成Ca(OH)2,不能确定是新生成的Ca(OH)2使酚酞变红还是样品中的Ca(OH)2使酚酞变红.
(2)请你结合本探究过程,写出一个你关心的问题:不一定不含Fe2O3.
 红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.提出问题:久置固体的成分是什么?
查阅资料:铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
作出猜想:久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
久置固体中可能含有Ca(OH)2的原因是:
用化学方程式表示CaO+H2O=Ca(OH)2.
实验探究1:甲同学的方案(见表).
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红 | 固体中一定含有和氢氧化钙 |
| (2)另取少量固体放于试管中,滴加足量的 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液 | 固体中一定含有,一定不含有Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清石灰水中 | 澄清石灰水变浑浊 | 固体中一定含有CaCO3 |
(1)乙同学认为甲同学的实验中的实验中不能得出一定含有Ca(OH)2的结论,理由是因为CaO会与水反应生成Ca(OH)2,不能确定是新生成的Ca(OH)2使酚酞变红还是样品中的Ca(OH)2使酚酞变红.
(2)请你结合本探究过程,写出一个你关心的问题:不一定不含Fe2O3.
14.下列物质中,属于有机化合物的是( )
| A. | 干冰 | B. | 碳酸钙 | C. | 纤维素 | D. | 金刚石 |
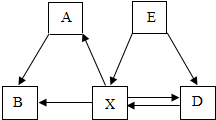 初中化学中几种常见物质之间的相互转化关系如图所示(每个字母各代表一种物质,每个箭头表示一个转换关系,部分反应物、生成物及反应条件略去)已知常温下B为气体,是植物进行光合作用的一种重要原料;D和E常温下均为无
初中化学中几种常见物质之间的相互转化关系如图所示(每个字母各代表一种物质,每个箭头表示一个转换关系,部分反应物、生成物及反应条件略去)已知常温下B为气体,是植物进行光合作用的一种重要原料;D和E常温下均为无 我国原油对外进口的依存度2013年是57%,而且以每年增长率为4%的速度递增,解决能源问题非常紧迫.太阳能的利用极大地解决了化石资源面临耗尽的问题,请回答有关问题:
我国原油对外进口的依存度2013年是57%,而且以每年增长率为4%的速度递增,解决能源问题非常紧迫.太阳能的利用极大地解决了化石资源面临耗尽的问题,请回答有关问题:
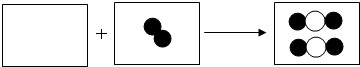 某同学组织化学兴趣小组的学生到郊外野炊.
某同学组织化学兴趣小组的学生到郊外野炊. 表示氧原子,
表示氧原子, 表示碳原子).
表示碳原子).