题目内容
游泳池里的水常加入适量的CuSO4用来杀灭其中的细菌,而对游泳者的身体无害.现取一水样300mL,经分析其中含有0.0192g Cu2+,则水样中CuSO4的物质的量浓度是多少?
考点:有关溶质质量分数的简单计算
专题:溶液的组成及溶质质量分数的计算
分析:先根据n=
计算铜离子的物质的量,再根据铜离子与硫酸铜之间的关系计算硫酸铜的物质的量.根据C=
计算硫酸铜的物质的量浓度.
| m |
| M |
| n |
| V |
解答:解:M(Cu2+)=64g/mol
n(CuSO4)=n(Cu2+)=
=
=0.0003mol
c(CuSO4)=
=
=0.001mol/L
答:水样中CuSO4的物质的量浓度是0.001mol/L.
n(CuSO4)=n(Cu2+)=
| m(Cu2+) |
| M(Cu2+) |
| 0.0192g |
| 64g/mol |
c(CuSO4)=
| n(CuSO4) |
| V |
| 0.0003mol |
| 0.3L |
答:水样中CuSO4的物质的量浓度是0.001mol/L.
点评:本题考查了物质的量浓度的有关计算,难度不大,明确铜离子和硫酸铜化学式之间的关系是解本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

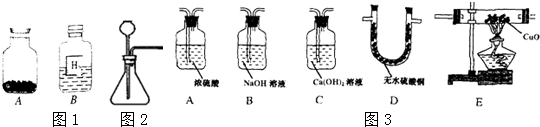
 如图是实验室电解水的简易装置示意图,试回答下列问题:
如图是实验室电解水的简易装置示意图,试回答下列问题: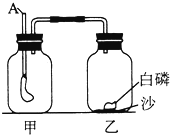 实验装置如图,甲、乙两个集气瓶用导管连接,玻璃管A的下端紧系一只气球.将此装置放置在阳光下一段时间后,可能观察到的现象是甲
实验装置如图,甲、乙两个集气瓶用导管连接,玻璃管A的下端紧系一只气球.将此装置放置在阳光下一段时间后,可能观察到的现象是甲