题目内容
15.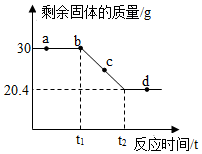 加热一定量氯酸钾和二氧化锰的混合物,固体质量与反应时间曲线如图.下列说法正确的是( )
加热一定量氯酸钾和二氧化锰的混合物,固体质量与反应时间曲线如图.下列说法正确的是( )| A. | 反应共生成氧气9.6g | |
| B. | 剩余固体20.4g为MnO2的质量 | |
| C. | 整个过程中有两种元素质量分数变大 | |
| D. | 原来混合固体中氯酸钾的质量分数为81.7% |
分析 氯酸钾在二氧化锰的催化作用下在加热条件下生成氯化钾和氧气,结合质量守恒定律、二氧化锰作催化剂(反应前后质量不变),进行分析判断.
解答 解:A、反应共生成氧气的质量为30g-20.4g=9.6g,故说法正确.
B、剩余固体20.4g为生成的氯化钾和MnO2的质量,故说法错误.
C、氯酸钾在二氧化锰的催化作用下在加热条件下生成氯化钾和氧气,反应后氧气逸出,由于二氧化锰中锰元素的质量不变,因此锰元素的质量分数增大,故说法错误.
D、设原来固体中氯酸钾的质量为x,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
x 9.6g
$\frac{245}{96}$=$\frac{x}{9.6g}$,
x=24.5g,原来混合固体中氯酸钾的质量分数为$\frac{24.5g}{30g}$×100%=81.7%,故选项正确.
故选:AD.
点评 本题是一道图象坐标与化学知识相结合的综合题,解题的关键是结合所涉及的化学知识,正确分析各变化的过程,注意分析坐标轴表示的意义、曲线的起点、折点及变化趋势,进而确定正确的图象.

练习册系列答案
相关题目
5.学会质疑是一种重要的化学思维,以下四个“一定”中正确的是( )
| A. | 温度升高,微粒之间的空隙一定变大 | |
| B. | 只有一种生成物的反应一定是化合反应 | |
| C. | 物质和氧气发生的反应,一定是氧化反应 | |
| D. | 某种气体密度大于空气,一定可以用向上排空气法收集 |
3.鉴别日常生活中的下列各组物质,正确的是( )
| A. | 硬水和软水:滴加食盐水 | B. | 氮气和二氧化碳:燃着的小木条 | ||
| C. | 水和过氧化氢溶液:加入二氧化锰 | D. | 生石灰和石灰石:高温锻烧 |
10.下列实验操作中正确的是( )
| A. |  熄灭酒精灯 | B. |  称量石灰石 | C. | 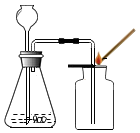 制取并验证CO2 | D. | 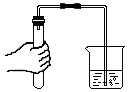 检查气密性 |
4.化学方程式是世界通用的化学语言,下列化学方程式正确的是( )
| A. | Mg+O2$\frac{\underline{\;\;△\;\;}}{\;}$MgO2 | B. | 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+O2↑ | ||
| C. | 2NaOH+SO2═Na2SO4+H2O | D. | BaCl2+Na2CO3═BaCO3↓+2NaCl |