题目内容
下列说法正确的是
A.玻璃钢和碳纤维是天然材料 B.钢铁在海水中不易锈蚀
C.白色物质造成的污染称为白色污染 D.用灼烧的方法区别棉花和羊毛
D

某实验小组对实验室制取氢气的反应原理进行探究。
【知识回顾】能产生氢气的化学反应有: ①水电解 ②活泼金属与酸反应
【讨论交流】反应①的化学方程式 ;同学们讨论后认为该反应不适用于实验室制取氢气。
【实验探究】为了探究哪种物质更适合用于实验室制取氢气,大家设计了如下实验:
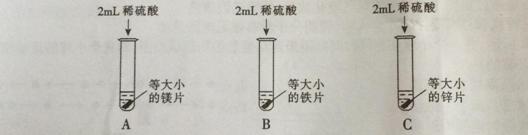
【分析与结论】填写实验报告。
| 实验 | 实验现象 | 实验结论 |
| A | 剧烈反应,迅速产生大量气泡,试管外壁 | 反应速率过快,气体不便收集,不能用于实验室制取氢气 |
| B | 缓慢产生少量气泡 | 反应速率过慢,不能用于实验室制取氢气 |
| C |
较快产生大量气泡,试管外壁发热 |
|
通过实验得出,适合实验室制取氢气的化学反应方程式为 ;
【知识拓展】(1)确定实验室制取气体的反应原理时,要考虑诸多因素,如反应的快慢、收集的难易、 等。
(2)用稀硫酸制取氢气时,制得的气 体中可能会增加的杂质为 。
体中可能会增加的杂质为 。
 某学习小组对课本中“食盐常用于制氯气、烧碱”
某学习小组对课本中“食盐常用于制氯气、烧碱”
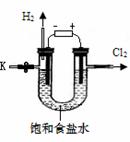
的内容产生兴趣。在老师的指导下,用自制的实验装置(主
体部分如右图所示)进行电解饱和食盐水制取氢氧化钠的实
验。一段时间后,关闭电源,从K处导出部分的溶液作为待
测液进行如下探究。
老师提示:I. 电解饱和食盐水的化学方程式:
2NaCl + 2H2O  2NaOH + H2↑+ Cl2↑
2NaOH + H2↑+ Cl2↑
II. 忽略其他可能发生的反应对以下实验的影响。
探究活动一:检验待测液中含有氢氧化钠
(1)同学们选用某种酸碱指示剂对待测液进行检验,请你将实验报告填写完整。
实验步骤 | 实验现象 | 实验结论 |
|
| 待测液呈碱性,表明含有氢氧化钠 |
探究活动二:测定待测液中氢氧化钠的质量分数
【实验1】用酸碱中和法测定
甲组同学称取一定质量的待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加
入一定溶质质量分数的稀盐酸,边加边振荡,用pH计测定溶液的pH,所得数据
如下:
加入稀盐酸的体积/mL | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 9.8 |
烧杯中溶液的pH | 13.0 | 12.9 | 12.8 | 12.6 | 12.3 | 7.0 |
(2)写出氢氧化钠与稀盐酸反应的化学方程式: 。
(3)利用氢氧化钠与稀盐酸恰好完全反应时的实验数据,计算所称取待测液中氢氧化钠的质量,应从选用稀盐酸的体积为 mL。
【实验2】用沉淀法测定
资料摘要:氢氧化钠与氯化镁溶液中发生反应:2NaOH+MgCl2=Mg(OH)2↓+2NaCl
乙组同学按下图所示的实验步骤进行实验:

(4)步骤②加入的氯化镁溶液必需足量,其目的是 。滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,
(写出实验步骤、现象和结论)。
(5)步骤③过滤出的沉淀物是 。
(6)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所
测定氢氧化钠的质量分数将 (选填“偏大”、“偏小”或“没影响”)。
