题目内容
1.分别将下列各组物质同时加到足量的水中,能得到无色透明溶液的是( )| A. | NaNO3、Ba(OH)2、Na2CO3 | B. | H2SO4,NaNO3,Na2SO4 | ||
| C. | H2SO4,NaNO3,FeSO4 | D. | CaCl2,Na2SO4,BaCl2 |
分析 若物质之间相互交换成分,能结合成沉淀的则不能得到透明的溶液;本题还要注意能得到无色透明溶液,不能含有明显有颜色的铜离子、铁离子和亚铁离子等.
解答 解:物质加到水中得到无色透明溶液,说明彼此之间不能生成沉淀,且不存在有色离子.
A、Ba(OH)2、Na2CO3在溶液反应生成碳酸钡白色沉淀,溶液变浑浊,不能得到无色透明溶液,故选项错误.
B、三者之间不反应,且不存在有色离子,符合无色透明的要求,故选项正确.
C、三者之间不反应,但FeSO4溶于水呈浅绿色,不能得到无色透明溶液,故选项错误.
D、Na2SO4、BaCl2在溶液反应生成硫酸钡白色沉淀,溶液变浑浊,不能得到无色透明溶液,故选项错误.
故选:B.
点评 本题难度不是很大,对于能否得到无色透明的溶液,要注意彼此之间不能生成沉淀,还要注意特定离子的颜色.

练习册系列答案
相关题目
12.小明同学为了寻找含碳酸钙质量分数超过85%的石灰石,对一样品进行了如表定量实验.
已知烧杯质量为13.1g,试通过计算分析:
(1)该试验中生成的二氧化碳的质量是4.4g.
(2)通过计算推断该是石灰石样品的纯度是否符合要求(石灰石样品中的杂质不与盐酸反应)?反应所得溶液的溶质质量分数是多少?(要求写出计算步骤)
| 实验步骤 | Ⅰ.将适量盐酸加入烧杯中并称重 | Ⅱ.称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应 | Ⅲ.待反应完全后,称重 |
| 实验图示 | 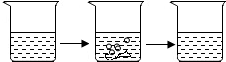 | ||
| 实验数据 | 烧杯和盐酸的质量为100.0g | 石灰石样品的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
(1)该试验中生成的二氧化碳的质量是4.4g.
(2)通过计算推断该是石灰石样品的纯度是否符合要求(石灰石样品中的杂质不与盐酸反应)?反应所得溶液的溶质质量分数是多少?(要求写出计算步骤)
6.化学方程式是重要的化学用语,下列化学方程式中正确的是( )
| A. | 2KClO3$\stackrel{MnO_2}{→}$2KCl+3O2↑ | B. | 3CO+Fe2O3$\stackrel{高温}{→}$2Fe+3CO2 | ||
| C. | NaCl+H2O→NaOH+HCl | D. | 2NaOH+SO2→Na2SO4+H2O |
13.下列物质中,属于无机物的是( )
| A. | 水 | B. | 淀粉 | C. | 蔗糖 | D. | 葡萄糖 |
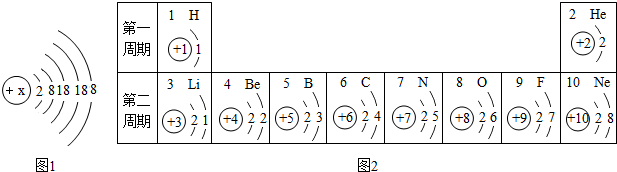
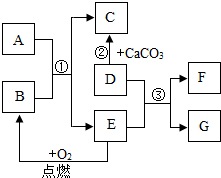 物质A-G均为初中化学常见物质,其相互转化关系如图所示(部分反应物、生成物、反应条件已略去)已知A、E为单质,且E为世界上用量最大的金属,C为植物进行光合作用的原料.
物质A-G均为初中化学常见物质,其相互转化关系如图所示(部分反应物、生成物、反应条件已略去)已知A、E为单质,且E为世界上用量最大的金属,C为植物进行光合作用的原料.