题目内容
5.下列实验操作正确的是( )| A. | 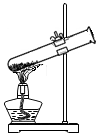 加热胆矾固体 | B. | 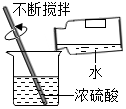 稀释浓硫酸 | ||
| C. | 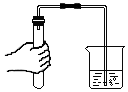 检查装置的气密性 | D. | 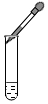 滴加液体试剂 |
分析 A、根据给试管中的固体加热的方法进行分析判断.
B、根据浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)进行分析判断.
C、根据检查装置气密性的方法进行分析判断.
D、用胶头滴管滴加液体时胶头滴管应垂直悬空,不能伸入试管内.
解答 解:A、给试管中的固体加热时,为防止液体倒流回试管,试管口要向下倾斜,图中所示操作错误.
B、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;图中所示操作错误.
C、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气;图中所示操作正确.
D、用胶头滴管滴加液体时胶头滴管应垂直悬空,不能伸入试管内,图中所示操作错误;
故选:C.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.下列属于物理变化的是( )
| A. | 切开苹果后,切面不久变黑 | B. | 食物腐败变质 | ||
| C. | 石油通过蒸馏制取汽油 | D. | 铁丝在潮湿的空气中生锈 |
20.分类是学习和研究化学的常用方法,下列物质分类正确的是( )
| A. | 混合物:矿泉水、纯净的空气 | B. | 酸:盐酸、硫酸铜 | ||
| C. | 氧化物:水、氢氧化钠 | D. | 有机物:葡萄糖、二氧化碳 |
17.如图,甲和乙分别是氢气和一氧化碳还原氧化铜的实验,下列有关说法正确的是( )


| A. | 甲实验试管口向下倾斜可防止氢气逸出 | |
| B. | 乙实验只能通过澄清石灰水是否变浑浊判断反应是否发生 | |
| C. | 甲、乙两实验中,都应先通入气体,再使试管、玻璃管均匀受热,以防止发生爆炸 | |
| D. | 甲、乙两实验中,氢气和一氧化碳都将氧化铜变成游离态的铜,都发生了置换反应 |
14.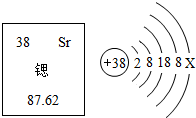 锶元素在元素周期表中的信息与锶原子结构示意图如图所示,下列说法错误的是( )
锶元素在元素周期表中的信息与锶原子结构示意图如图所示,下列说法错误的是( )
 锶元素在元素周期表中的信息与锶原子结构示意图如图所示,下列说法错误的是( )
锶元素在元素周期表中的信息与锶原子结构示意图如图所示,下列说法错误的是( )| A. | Sr为金属元素 | B. | 乙图中X≡3 | ||
| C. | 锶原子的质量为87.62g | D. | 锶原子的质子数是38 |
15. 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
(1)写出镁条与氧气反应化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律.我不同意(“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小红按如图所示装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】
①氧化镁为白色固体;
②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【设计实验】验证黄色固体为Mg3N2,请完成下列实验报告.
【反思交流】
①实验中,小气球的作用是形成密封体系,平衡气压.
②空气中N2的含量大于O2的含量,而镁条在空气之中燃烧生成的氧化镁却远多于氮化镁,为什么?请给出合理的解释氧气的化学性质比氮气更活泼,镁条更容易与氧气发生反应.
 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.(1)写出镁条与氧气反应化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律.我不同意(“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小红按如图所示装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】
①氧化镁为白色固体;
②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【设计实验】验证黄色固体为Mg3N2,请完成下列实验报告.
| 操作步骤 | 实验现象 | 实验结论 |
| 取少量黄色固体于试管中,加入适量的水,并将湿润的红色石蕊试纸放在试管口 | 试管中有气体产生,湿润的红色石蕊试纸变蓝 | 黄色固体为Mg3N2 |
①实验中,小气球的作用是形成密封体系,平衡气压.
②空气中N2的含量大于O2的含量,而镁条在空气之中燃烧生成的氧化镁却远多于氮化镁,为什么?请给出合理的解释氧气的化学性质比氮气更活泼,镁条更容易与氧气发生反应.
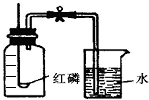 通过实验现象和题给信息,按要求填空.为测定空气的成分按如图进行实验:
通过实验现象和题给信息,按要求填空.为测定空气的成分按如图进行实验: