题目内容
4.下列实验现象不正确的是( )| A. | 打开浓盐酸的试剂瓶盖,瓶口会出现白雾 | |
| B. | 生锈的铁钉放入少量无色稀硫酸中溶液变黄色 | |
| C. | 一氧化碳在空气中燃烧发出蓝色火焰 | |
| D. | 氯酸钾与二氧化锰混合后,即可产生大量氧气 |
分析 A、根据盐酸的挥发性解答;
B、根据铁锈的成分与硫酸的反应解答;
C、根据一氧化碳的燃烧火焰解答;
D、根据硫酸钾与二氧化锰的混合加热解答.
解答 解:A、浓盐酸具有挥发性,挥发出的氯化氢气体能与空气中的水蒸气形成盐酸小液滴,故打开浓盐酸的试剂瓶盖,瓶口会出现白雾,正确;
B、生锈的铁钉放入少量无色稀硫酸中,硫酸与铁锈的成分氧化铁反应生成硫酸铁和水,硫酸铁的水溶液为黄色,故溶液变黄色,正确;
C、一氧化碳在空气中燃烧发出蓝色火焰,正确;
D、氯酸钾与二氧化锰混合后加热一会才产生大量氧气,错误;
故选D.
点评 本题考查的是常见的化学实验现象,完成此题,可以依据已有的物质的性质进行.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
19.下列装置能达到对应实验目的是( )
| A. |  比较 MnO2和 Fe2O3的催化效果 | B. | 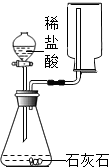 制取并收集CO2气体 | ||
| C. | 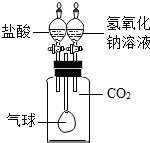 证明 CO2和 NaOH已发生反应 | D. |  形成蓝色喷泉 |
9.下表列出了除去物质中所含少量杂质的方法,其中不正确的选项是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | FeCl2溶液 | CuCl2溶液 | 加入过量的铁粉,过滤 |
| B | CaCO3粉末 | NaCl粉末 | 加水溶解、过滤、洗涤、烘干 |
| C | 氯化钾 | 氯酸钾 | 加热 |
| D | 氢氧化钠溶液 | 氢氧化钙溶液 | 通入CO2,过滤 |
| A. | A | B. | B | C. | C | D. | D |
13.“民以食为天”.下列食物或食品中,含有丰富蛋白质的是( )
| A. | 冰激凌 | B. | 拔丝苹果 | C. | 红烧牛肉 | D. | 糖醋黄瓜 |
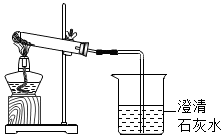 请你参与某校九年级(1)班化学研究性学习小组的探究活动,并回答相关问题.
请你参与某校九年级(1)班化学研究性学习小组的探究活动,并回答相关问题.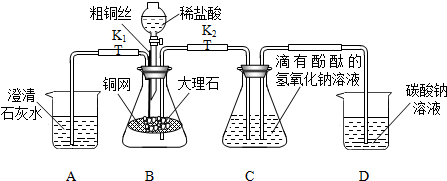
 实验室制取气体时所需的一些装置如图所示,请回答下列问题:
实验室制取气体时所需的一些装置如图所示,请回答下列问题: