题目内容
12.下列说法正确的是( )| A. | 原子团在化学反应中,有时是可以拆开的 | |
| B. | 配平化学方程式时,有时可改动化学式中的小字码,但不常用 | |
| C. | 化学方程式配平是为了计算的方便 | |
| D. | 化学方程式中的“↓”表示生成是固体,因此反应中只要有固体生成就必须标示“↓” |
分析 A、根据原子团在化学变化中的变化,进行分析判断.
B、配平时要注意化学计量数必须加在化学式的前面,配平过程中不能改变化学式中的下标.
C、根据质量守恒定律,进行分析判断.
D、根据化学方程式配平的注意事项,进行分析判断.
解答 解:A、原子团在化学反应中,有时是可以拆开的,如2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,ClO3被拆开,故选项说法正确.
B、配平化学方程式时,不能改动化学式中的小字码,故选项说法错误.
C、化学方程式配平是为了使反应遵守质量守恒定律,故选项说法错误.
D、化学方程式中的“↓”表示生成是固体,但并不是反应中只要有固体生成就必须标示“↓”,反应物中有固体时,生成物固体的后面不需要标示“↓”,故选项说法错误.
故选:A.
点评 本题难度不大,掌握化学方程式的配平方法、注意事项等是正确解答本题的关键.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
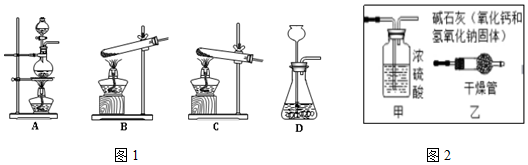
12.小敏和小玉在实验室用盐酸和石灰石反应,分别用甲、乙装置(气密性均良好)进行二氧化碳的制取及性质实验,但均未发现澄清石灰水变浑浊,针对此现象,同学们提出了自己的想法,小敏同学实验时澄清石灰水未变混浊的原因是产生的气体从长颈漏斗中逸出.
【提出问题】小玉同学实验时澄清石灰水为什么没有变浑浊呢?
【作出猜想】猜想一:澄清石灰水变质.猜想二:反应产生的气体除了有二氧化碳外,还有氯化氢.
【查阅资料】氯化氢气体溶于水形成盐酸.
【实验探究】

同学们经过讨论发现,用丙装置(如图)在A、B中均加入实验Ⅱ所用试剂即可同时完成上述两个猜想的探究,其中B装置所起的作用是检验氯化氢气体是否除尽,如果看到A中有白色沉淀产生,B,C中无变化的现象,则两个猜想都成立.
【实验反思】由实验可知,小玉同学实验时可能错误使用了一种药品,她实验的药品是浓盐酸.
【提出问题】小玉同学实验时澄清石灰水为什么没有变浑浊呢?
【作出猜想】猜想一:澄清石灰水变质.猜想二:反应产生的气体除了有二氧化碳外,还有氯化氢.
【查阅资料】氯化氢气体溶于水形成盐酸.
【实验探究】

| 实验 | 实验步骤 | 实验现象 | 实验结论 |
| 实验Ⅰ | 将纯净的CO2通入到该实验所用的澄清石灰水中 | 澄清石灰水变浑浊 | 猜想一不成立 |
| 实验Ⅱ | 将反应产生的气体通入到硝酸银溶液中 | 有白色沉淀产生 | 猜想二成立 |
【实验反思】由实验可知,小玉同学实验时可能错误使用了一种药品,她实验的药品是浓盐酸.
3.质量守恒定律是帮助我们学习和认识化学反应实质的重要理论.
(1)下列表述正确的是B.
A.蜡烛燃烧后质量减少,说明质量守恒定律不是普遍规律
B.每32g S和32g O2完全反应后,生成64g SO2
C.在化学反应aA+bB══cC+dD中一定有:a+b=c+d
(2)有机化合物R与足量氧气置于密闭容器中充分反应生成CO2和H2O,实验测得反应前后物后的质量如表,
则x=88;已知参加反应的物质R与氧气的分子个数之比为1:3.则R的相对分子质量是46.
(1)下列表述正确的是B.
A.蜡烛燃烧后质量减少,说明质量守恒定律不是普遍规律
B.每32g S和32g O2完全反应后,生成64g SO2
C.在化学反应aA+bB══cC+dD中一定有:a+b=c+d
(2)有机化合物R与足量氧气置于密闭容器中充分反应生成CO2和H2O,实验测得反应前后物后的质量如表,
| R | O2 | CO2 | H2O | |
| 反应前质量/g | 46 | 128 | 0 | 0 |
| 反应后质量/g | 0 | 32 | x | 54 |
7.下列各组物质中,前者属于混合物、后者属于单质的是( )
| A. | 蒸馏水 氮气 | B. | 二氧化碳 氢气 | C. | 大理石 空气 | D. | 石油 氧气 |
1.地壳中含量最多的三种金属元素,按含量由多到少顺序的排列的是( )
| A. | 镁、铝、铁 | B. | 银、铜、铝 | C. | 铝、铁、钙 | D. | 钙、铝、铁 |
2.生活中常见的下列现象中,都属于化学变化的一组是( )
| A. | 汽油挥发 酒精燃烧 | B. | 食物腐烂 钢铁生锈 | ||
| C. | 蜡烛燃烧 铁铸成锅 | D. | 水分蒸发 滴水成冰 |