题目内容
16.磁悬浮的核心技术需制备超导材料,有一种超导材料的化学式是Fe2BaCu6O10,它是以Fe2O3、BaCO3和CuO为原料经研磨烧结而成.请完成下列计算:(1)该超导材料是由四 种元素组成的.
(2)BaCO3的相对分子质量是197,CuO中铜元素与氧元素的质量比为4:1.
(3)求Fe2O3中氧元素的质量分数(写出计算过程)
分析 (1)根据化学式的意义来分析;
(2)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答;
(3)根据化合物中元素的质量分数计算方法来分析.
解答 解:(1)由化学式可知Fe2BaCu6O10,该材料是由铁、钡、铜和氧四种元素组成的,故填:四;
(2)BaCO3的相对分子质量是:137+12+16×3=197;
CuO中铜元素与氧元素的质量比为:64:16=4:1;故填:197;4:1;
(3)Fe2O3中氧元素的质量分数=$\frac{16×3}{56×2+16×3}×100%$=30%;故填:30%.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.国际互联网上报道:目前有近20亿人患有缺铁性贫血,这里的“铁”是指( )
| A. | 金属铁 | B. | 铁元素 | C. | 铁锈 | D. | 四氧化三铁 |
4.薯片等易碎食品宜采用充气包装,下列气体中最适宜充入气体的是( )
| A. | 空气 | B. | N2 | C. | O2 | D. | 稀有气体 |
1.如图是某兴趣小组设计的四个实验装置,其中实验操作设计正确的是( )
| A. | 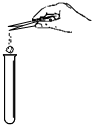 向试管加固体 | B. | 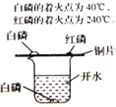 探究可燃物燃烧的条件 | ||
| C. | 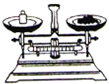 称量氯化钠 | D. | 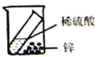 验证质量守恒定律 |
8.下列化学反应中属于分解反应的是( )
| A. | 高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气 | |
| B. | 石蜡+氧气$\stackrel{点燃}{→}$水+二氧化碳 | |
| C. | 铁+氧气$\stackrel{点燃}{→}$四氧化三铁 | |
| D. | 硫+氧气$\stackrel{点燃}{→}$二氧化硫 |