题目内容
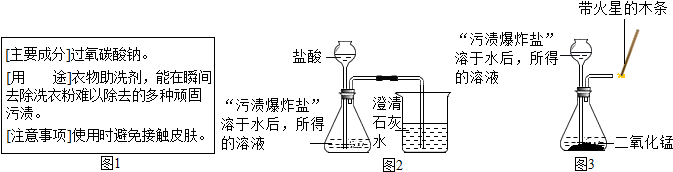
8.小明同学对超市一种新产品--“污渍爆炸盐”有关问题进行探究.该产品的说明书如图1:
查阅查阅资料
得知:过氧碳酸钠(Na2CO4) 俗称“固体双氧水”,白色结晶颗粒.
“污渍爆炸盐”溶于水后,Na2CO4与H2O反应只生成2种物质,1种是碳酸盐,另1种化合物A.
(1)根据以上信息推断,“污渍爆炸盐”溶于水后,生成的碳酸盐是碳酸钠(写物质名称).
(2)为了验证“污渍爆炸盐”溶于水后有碳酸盐生成,小明按图2所示进行实验.观察到锥形瓶内有气泡放出,烧杯中澄清石灰水变浑浊.则烧杯中反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.该反应的基本反应类型是复分解反应.
(3)为了探究“污渍爆炸盐”溶于水后生成另化合物A是什么,小明设计并进行实验(如图3所示).观
察到锥形瓶内有气泡放出,带火星的木条复燃.则化合物A为过氧化氢(或H2O2),A在二氧化锰催化作用下发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(4)你认为“污渍爆炸盐”应密封保存.
分析 (1)根据信息“污渍爆炸盐”溶于水后,Na2CO4与H2O反应只生成2种物质,1种是碳酸盐,另1种是化合物A,结合质量守恒定律分析;
(2)根据烧杯中澄清石灰水变浑浊,写出二氧化碳与氢氧化钙反应的方程式;
(3)根据观察到锥形瓶内有气泡放出,带火星的木条复燃,得出化合物A是过氧化氢,写出方程式,二氧化锰是催化剂;
(4)根据“污渍爆炸盐”的性质回答保存方法.
解答 解:(1)“污渍爆炸盐”溶于水后,Na2CO4与H2O反应只生成2种物质,其中1种是碳酸盐,依据反应前后元素的种类不变,可知是碳酸钠;
(2)烧杯中澄清石灰水变浑浊,说明是碳酸钠与盐酸反应产生的二氧化碳与氢氧化钙反应的结果,因此方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;该反应的基本反应类型是复分解反应;
(3)观察到锥形瓶内有气泡放出,且带火星的木条复燃,说明是过氧化氢溶液与二氧化锰作用产生氧气的结果,故A是过氧化氢,反应的方程式为:2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(4)“污渍爆炸盐”容易与水反应,故应该密封保存;
故答案为:
(1)碳酸钠;
(2)CO2+Ca(OH)2═CaCO3↓+H2O;复分解反应;
(3)过氧化氢(或H2O2); 2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(4)密封.
点评 本题属于信息题的考查,关键是明确氧气和二氧化碳的检验方法,掌握过氧化氢和碳酸钠的性质,能够根据物质的性质来选择合适的方法来对物质加以验证等,本题型的特点是起点高,但落点低.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
13.空气中氧气含量测定的再认识.
【经典赏析】教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图1).该实验中选择使用汞的优点有BCD.
A.实验过程中没有污染
B.在汞槽中起到液封作用
C.生成的化合物加热分解又能得到汞和氧气
D.能将密闭装置内空气中的氧气几乎耗尽
【实验回顾】实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图2),写出红磷燃烧的化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.兴趣小组用该方法测出的氧气含量常常远低于21%.
【提出问题】用红磷燃烧的方法为什么不能准确地测定空气中氧气的含量?
【进行猜想】(1)装置漏气;(2)红磷不足装置内氧气有剩余;…
【实验与交流】在老师的指导下,小明分别用过量的红磷和白磷进行该实验,用测氧气浓度的传感器测得反应后装置内氧气浓度分别为8.85%和3.21%,请从燃烧条件的角度回答产生上述结果的主要原因白磷的着火点比红磷的着火点低.
【实验探究1】小明根据铁生锈的原理,探究用铁能否准确测定空气中氧气的含量,于是进行了实验(装置如图3)通过7天测得的数据计算空气中氧气的含量为19.13%.
【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点及原因:装置内残留的氧气更少,实验结果更准确.
【实验探究2】为了加快反应速率,小明通过查阅资料,利用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图4),8分钟后测得的数据如表:
请计算出空气中氧气含量20.2%(计算结果保留一位小数)
【结论与反思】通过上述实验探究,选择铁粉、炭粉、氯化钠和蒸馏水(填物质名称)进行实验,可较为快速地完成实验并减小实验误差.
【拓展延伸】铜也能与空气中氧气、水、二氧化碳反应而锈蚀,生成铜绿[铜绿的主要成分为Cu2(OH)2CO3],若将图3装置中的粗铁丝换成足量的铜丝进行实验,请判断能否比较准确地测定空气中氧气的含量,并说明理由.不能;因为空气中二氧化碳含量约只有0.03%,铜不能将装置中的氧气几乎耗尽.
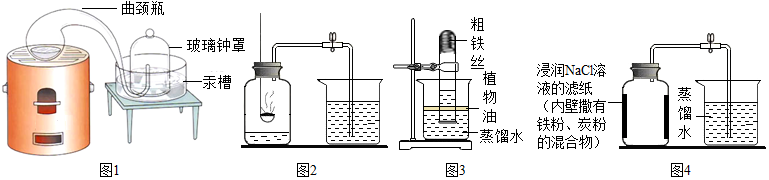
【经典赏析】教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图1).该实验中选择使用汞的优点有BCD.
A.实验过程中没有污染
B.在汞槽中起到液封作用
C.生成的化合物加热分解又能得到汞和氧气
D.能将密闭装置内空气中的氧气几乎耗尽
【实验回顾】实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图2),写出红磷燃烧的化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.兴趣小组用该方法测出的氧气含量常常远低于21%.
【提出问题】用红磷燃烧的方法为什么不能准确地测定空气中氧气的含量?
【进行猜想】(1)装置漏气;(2)红磷不足装置内氧气有剩余;…
【实验与交流】在老师的指导下,小明分别用过量的红磷和白磷进行该实验,用测氧气浓度的传感器测得反应后装置内氧气浓度分别为8.85%和3.21%,请从燃烧条件的角度回答产生上述结果的主要原因白磷的着火点比红磷的着火点低.
【实验探究1】小明根据铁生锈的原理,探究用铁能否准确测定空气中氧气的含量,于是进行了实验(装置如图3)通过7天测得的数据计算空气中氧气的含量为19.13%.
【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点及原因:装置内残留的氧气更少,实验结果更准确.
【实验探究2】为了加快反应速率,小明通过查阅资料,利用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图4),8分钟后测得的数据如表:
| 实验前的体积 | 实验后的体积 | |
| 集气瓶内空气 | 烧杯内蒸馏水 | 烧杯内剩余蒸馏水 |
| 131mL | 90.0mL | 63.6mL |
【结论与反思】通过上述实验探究,选择铁粉、炭粉、氯化钠和蒸馏水(填物质名称)进行实验,可较为快速地完成实验并减小实验误差.
【拓展延伸】铜也能与空气中氧气、水、二氧化碳反应而锈蚀,生成铜绿[铜绿的主要成分为Cu2(OH)2CO3],若将图3装置中的粗铁丝换成足量的铜丝进行实验,请判断能否比较准确地测定空气中氧气的含量,并说明理由.不能;因为空气中二氧化碳含量约只有0.03%,铜不能将装置中的氧气几乎耗尽.

13.有一包固体粉末,其中含有碳酸钠、氢氧化钠、碳酸钙、生石灰、氯化钠中的四种物质.某兴趣小组为确定其组成设计并进行如下实验.
【实验一】甲组同学进行如下探究.请完成表中空白.
【实验二】乙组同学进行如下探究.
取21.0g该固体粉末,加入160.0g 10%的稀盐酸,恰好完全反应,实验测得产生8.8g二氧化碳,将反应后溶液继续蒸发结晶,得到固体,测定所得固体中含16.0g氯元素.
试综合甲、乙两组同学的实验进行分析,填空:
(1)乙组实验中一定发生的化学反应是:Na2C03+2HCl═2NaCl+H20+C02↑
(2)固体粉末的组成中除Na2C03外,一定还含有的物质是CaC03、NaCl,可能含有的物质是Ca0、Na0H(均填写化学式)
【实验一】甲组同学进行如下探究.请完成表中空白.
| 实验操作 | 实验现象 | 实验结论及分析 | |
| Ⅰ.取少量该固体粉末于烧杯中,加入足量的水溶解、过滤 | 粉末部分溶解,得到白色滤渣和无色滤液 | 滤渣中一定含有碳酸钙 | |
| Ⅱ.向滤液中滴加无色酚酞试液 | 溶液变红 | 滤液中可能含有碱性物质(填“酸性”“碱性”或“中性”) | |
| Ⅲ.向Ⅱ中所得溶液滴加足量稀盐酸 | 有气泡生成 | 原固体粉末中一定含有Na2CO3 | |
取21.0g该固体粉末,加入160.0g 10%的稀盐酸,恰好完全反应,实验测得产生8.8g二氧化碳,将反应后溶液继续蒸发结晶,得到固体,测定所得固体中含16.0g氯元素.
试综合甲、乙两组同学的实验进行分析,填空:
(1)乙组实验中一定发生的化学反应是:Na2C03+2HCl═2NaCl+H20+C02↑
(2)固体粉末的组成中除Na2C03外,一定还含有的物质是CaC03、NaCl,可能含有的物质是Ca0、Na0H(均填写化学式)
20.“关爱生命,关注健康”是现代人类的生活理念,下列符合这一理念的是( )
| A. | 为缓解驾驶疲劳,建议司机抽烟提神 | |
| B. | 误服重金属盐中毒,可服用鸡蛋清解毒 | |
| C. | 烧制海鲜,先用甲醛浸泡除异味且增强口感 | |
| D. | 为预防得夜盲症,儿童需要适当补充维生素C药片 |
17. 春节期间,小颖陪妈妈去医院打点滴,发现护士往输液管上放了一个纸包,经询问得知它是输液恒温贴,可以温暖输入人体中的液体.小颖对包里的东西能产生热量感到很神奇,于是,他向护士要了一只输液恒温贴,带回来进行了如下探究.撕开真空包装封口,剪开内包装袋,倒出其中的粉末,发现呈黑色.
春节期间,小颖陪妈妈去医院打点滴,发现护士往输液管上放了一个纸包,经询问得知它是输液恒温贴,可以温暖输入人体中的液体.小颖对包里的东西能产生热量感到很神奇,于是,他向护士要了一只输液恒温贴,带回来进行了如下探究.撕开真空包装封口,剪开内包装袋,倒出其中的粉末,发现呈黑色.
【提出问题】黑色粉末可能含有哪些物质呢?
【猜想与假设】该黑色粉末可能含有炭粉、铁粉、二氧化锰、氧化铜、四氧化三铁中的一种或几种.
【初步验证】将磁铁靠近黑色粉末,部分被吸引.
【查阅资料】四氧化三铁能被磁铁吸引.四氧化三铁与盐酸反应生成氯化亚铁、氯化铁和水.
【初步结论】黑色粉末可能含有Fe3O4(或Fe).
【进行实验】
由上述实验可知,该黑色粉末肯定含有Fe和C,肯定不含CuO;写出实验①中产生气体的化学方程式Fe+H2SO4═FeSO4+H2↑.
【交流讨论】①输液恒温贴真空包装的原因:铁粉在空气中会与水和氧气发生缓慢氧化转化成铁锈,并放出热量.
②输液恒温贴中炭粉的作用是加快铁粉生锈.
 春节期间,小颖陪妈妈去医院打点滴,发现护士往输液管上放了一个纸包,经询问得知它是输液恒温贴,可以温暖输入人体中的液体.小颖对包里的东西能产生热量感到很神奇,于是,他向护士要了一只输液恒温贴,带回来进行了如下探究.撕开真空包装封口,剪开内包装袋,倒出其中的粉末,发现呈黑色.
春节期间,小颖陪妈妈去医院打点滴,发现护士往输液管上放了一个纸包,经询问得知它是输液恒温贴,可以温暖输入人体中的液体.小颖对包里的东西能产生热量感到很神奇,于是,他向护士要了一只输液恒温贴,带回来进行了如下探究.撕开真空包装封口,剪开内包装袋,倒出其中的粉末,发现呈黑色.【提出问题】黑色粉末可能含有哪些物质呢?
【猜想与假设】该黑色粉末可能含有炭粉、铁粉、二氧化锰、氧化铜、四氧化三铁中的一种或几种.
【初步验证】将磁铁靠近黑色粉末,部分被吸引.
【查阅资料】四氧化三铁能被磁铁吸引.四氧化三铁与盐酸反应生成氯化亚铁、氯化铁和水.
【初步结论】黑色粉末可能含有Fe3O4(或Fe).
【进行实验】
| 实验 编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末于试管中,加足量稀硫酸 | 固体部分溶解,有气泡产生,溶液变为浅绿色 |
| ② | 将实验①试管中的物质过滤,向滤液中加入足量铁粉 | 有气泡产生,无红色物质析出 |
| ③ | 取实验②的滤渣灼烧,将内壁涂有澄清石灰水的小烧杯罩在上方 | 澄清石灰水变浑浊 |
【交流讨论】①输液恒温贴真空包装的原因:铁粉在空气中会与水和氧气发生缓慢氧化转化成铁锈,并放出热量.
②输液恒温贴中炭粉的作用是加快铁粉生锈.
18.下列属于化学变化的是( )
| A. |  胆矾研碎 | B. |  干冰升华 | C. |  品红扩散 | D. |  蜡烛燃烧 |
 生活中出处处有化学.结合你所学的知识回答下列问题:
生活中出处处有化学.结合你所学的知识回答下列问题: