题目内容
13. 如图是a、b、c三种物质的溶解度曲线a与c的溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质的溶解度曲线a与c的溶解度曲线相交于P点.据图回答:(1)曲线a和c的交点P表示的含义是t1℃时,a、c的溶解度相等,是20g.
(2)0℃时,a、b、c三种物质中溶解度最大的是c.
(3)t1℃时,三种物质的饱和溶液升温至t2℃时,首先析出晶体的是c.
(4)t2℃时,将30ga物质加入50g水中充分溶解,所形成的溶液的溶质质量分数为33.3%.
分析 (1)溶解度曲线的交点表示该温度下两物质的溶解度相等;
(2)根据固体物质的溶解度曲线可以:比较不同的物质在0℃时的溶解度大小;
(3)根据固体物质的溶解度曲线可解答;
(4)固体物质的溶解度是指在一定的温度下,某固体物质在100克溶剂中达到饱和状态时所溶解的质量,则同温度下物质的饱和溶液中溶质的质量分数是$\frac{溶质质量}{溶液溶液}$×100%
解答 解:(1)交点P的含义是t1℃时,a、c的溶解度相等,是20g;
(2)由溶解度曲线知:0℃时,a、b、c三种物质的溶解度由小到的顺序是c>b>a,故溶解度最大的是c;
(3)由于c的溶解度随温度的升高而减小,因此给c的饱和溶液升温时,会有晶体析出,a、b的溶解度随温度的升高而增大,故无晶体析出;
(4)t2℃时,a的溶解度为50g,故50g水可溶解25ga,故$\frac{25g}{50g+25g}$×100%=33.3%.
故答案为:(1)t1℃时,a、c的溶解度相等,是20g;(2)c;(3)c;(4)33.3%.
点评 本题难度不是很大,主要考查了固体溶解度曲线的意义及固体溶解度概念的应用,培养学生分析问题、解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.乙醇(C2H5OH)是可再生资源,其燃烧的化学方程式为C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O,该化学方程式中,不存在的物质种类是( )
| A. | 单质 | B. | 氧化物 | C. | 酸 | D. | 有机化合物 |
1.t℃时,将一定量KNO3的不饱和溶液平均分为三份,分别恒温蒸发出水的质量为5g、10g,析出KNO3晶体的质量依次为2g、5g,第三份蒸干得到KNO3的晶体质量为12.5g,则每份溶液中所含水的量为( )
| A. | 12.5g | B. | 22.5g | C. | 25g | D. | 20.83g |
8.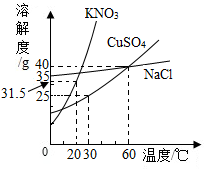 如图是几种盐的溶解度曲线,下列说法正确的是( )
如图是几种盐的溶解度曲线,下列说法正确的是( )
 如图是几种盐的溶解度曲线,下列说法正确的是( )
如图是几种盐的溶解度曲线,下列说法正确的是( )| A. | 40℃时,将35g食盐溶于100g水中,降温至0℃可析出NaCl晶体 | |
| B. | 20℃时,KNO3饱和溶液的质量分数 是31.5% | |
| C. | 60℃时,200g水中溶解80g硫酸铜达饱和,当降温至30℃可析出30g硫酸铜晶体 | |
| D. | 30℃时,将35gNaCl和35gKNO3同时溶于100g水中,蒸发时先析出NaCl |
5. 食醋是厨房中的一种调味品,其中含有少量醋酸.下列有关醋酸的说法不正确的是( )
食醋是厨房中的一种调味品,其中含有少量醋酸.下列有关醋酸的说法不正确的是( )
 食醋是厨房中的一种调味品,其中含有少量醋酸.下列有关醋酸的说法不正确的是( )
食醋是厨房中的一种调味品,其中含有少量醋酸.下列有关醋酸的说法不正确的是( )| A. | 醋酸分子是由碳、氢、氧三种原子构成的 | |
| B. | 醋酸中碳元素的质量分数为40% | |
| C. | 醋酸是由碳、氢、氧三种元素组成的 | |
| D. | 每个醋酸分子中有8个电子 |
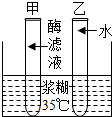 (1)为了探究酶的催化化作用,小王同学设计了如下的实验:取甲、乙两支洁净的试管,分别注入3毫升淀粉溶液,然后,在甲试管中注入2毫升新鲜的小麦淀粉酶滤液,在乙试管中注入2毫升清水,振荡两支试管.在接下来的下面三步操作中正确的顺序是②③①.
(1)为了探究酶的催化化作用,小王同学设计了如下的实验:取甲、乙两支洁净的试管,分别注入3毫升淀粉溶液,然后,在甲试管中注入2毫升新鲜的小麦淀粉酶滤液,在乙试管中注入2毫升清水,振荡两支试管.在接下来的下面三步操作中正确的顺序是②③①.