题目内容
某研究性学习小组对中和反应进行探究,请你参与实验: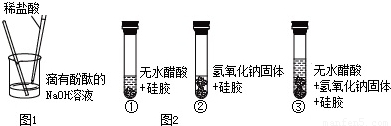
实验1:证明酸和碱发生了反应
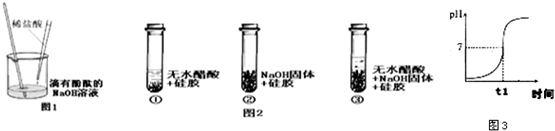
稀盐酸和NaOH溶液混合没有明显现象,小丽同学按图1进行实验,证明了盐酸和NaOH溶液有发生化学反应,他依据的实验现象是______.
实验2:证明酸和碱反应有水生成小明同学取变色硅胶(吸水后由蓝色变红色)、无水醋酸(一种酸,常温下为无色液体)和氢氧化钠固体进行图2所示的三个实验.
(1)实验①、②的实验目的是______.
(2)加入试剂后,要迅速塞紧橡胶塞的原因是______.
(3)能证明酸和碱反应有水生成的现象是______.
实验3:测量酸和碱反应过程的pH、温度变化
取一定量的稀盐酸,逐滴匀速滴加NaOH溶液,用传感器实时获得溶液的pH、温度曲线如图3.
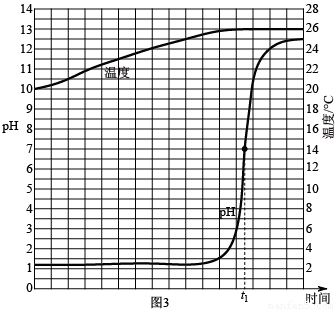
(1)0-t1时,溶液的酸碱性变化情况是______.
(2)由图3分析,酸和碱有发生反应的依据是______,酸和碱的反应是______反应(填“吸热”或“放热”).
【答案】分析:试验1、根据酚酞在酸、碱溶液中的颜色的变化分析;、
试验2、(1)根据硅胶的颜色的变化分析反应是否有有水生成;
(2)根据空气的成分分析;
(3)通过实验对比,硅胶颜色的变化分析;
试验3、观察图象,根据变化的趋势.分析溶液的酸碱性变化,能量的变化.
解答:解:试验1、无色酚酞试液在氢氧化钠溶液中显红色,滴入了稀盐酸变成了无色,说明了盐酸与氢氧化钠发生了反应;
试验2、(1)通过实验①、②的实验现象的对比证明了无水醋酸和氢氧化钠不含有水,不能使硅胶变色,由试验③硅胶的变色说明了中和反应有水生成.
(2)空气中含有水,也能使硅胶变色,迅速塞紧橡胶塞可防止空气中的水分进入试管干扰试验;
(3)能证明酸和碱反应有水生成的现象是:实验①②对比,③硅胶颜色的变化;
试验3、通过观察图象可以看出:(1)由pH曲线随着滴入的氢氧化钠的增多,酸性逐渐减弱,当t1时溶液呈中性;
(2)由pH曲线随着滴入的氢氧化钠的增多,pH增大,当t1时pH=7,说明了酸与碱发生了中和反应;由温度的变化曲线可以看出,曲线逐渐上升,说明了中和反应是放热反应.
答:试验1:滴有酚酞的氢氧化钠溶液由红色变成无色;
试验2、(1)证明了无水醋酸和氢氧化钠不含有水,不能使硅胶变色;(2)防止空气中的水分进入试管干扰试验;(3)试管③中的硅胶由蓝色变为红色,试管①②中的硅胶不变色.
试验3、(1)溶液酸性减弱,t1时溶液呈中性;
(2)溶液的pH增大,当t1时pH=7,放热.
点评:本题属于实验探究题,综合性较强,既有试验探究,又有实验数据图象的分析.只有综合掌握了基础知识才能较好的完成本类练习题.
试验2、(1)根据硅胶的颜色的变化分析反应是否有有水生成;
(2)根据空气的成分分析;
(3)通过实验对比,硅胶颜色的变化分析;
试验3、观察图象,根据变化的趋势.分析溶液的酸碱性变化,能量的变化.
解答:解:试验1、无色酚酞试液在氢氧化钠溶液中显红色,滴入了稀盐酸变成了无色,说明了盐酸与氢氧化钠发生了反应;
试验2、(1)通过实验①、②的实验现象的对比证明了无水醋酸和氢氧化钠不含有水,不能使硅胶变色,由试验③硅胶的变色说明了中和反应有水生成.
(2)空气中含有水,也能使硅胶变色,迅速塞紧橡胶塞可防止空气中的水分进入试管干扰试验;
(3)能证明酸和碱反应有水生成的现象是:实验①②对比,③硅胶颜色的变化;
试验3、通过观察图象可以看出:(1)由pH曲线随着滴入的氢氧化钠的增多,酸性逐渐减弱,当t1时溶液呈中性;
(2)由pH曲线随着滴入的氢氧化钠的增多,pH增大,当t1时pH=7,说明了酸与碱发生了中和反应;由温度的变化曲线可以看出,曲线逐渐上升,说明了中和反应是放热反应.
答:试验1:滴有酚酞的氢氧化钠溶液由红色变成无色;
试验2、(1)证明了无水醋酸和氢氧化钠不含有水,不能使硅胶变色;(2)防止空气中的水分进入试管干扰试验;(3)试管③中的硅胶由蓝色变为红色,试管①②中的硅胶不变色.
试验3、(1)溶液酸性减弱,t1时溶液呈中性;
(2)溶液的pH增大,当t1时pH=7,放热.
点评:本题属于实验探究题,综合性较强,既有试验探究,又有实验数据图象的分析.只有综合掌握了基础知识才能较好的完成本类练习题.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
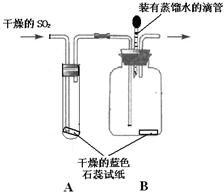 14、某研究性学习小组对“SO2能否与H2O反应生成酸”的课题开展探究.查阅资料后得知:
14、某研究性学习小组对“SO2能否与H2O反应生成酸”的课题开展探究.查阅资料后得知: