题目内容
17.氯酸钾(KClO3)可用于实验室里制取氧气,常加入二氧化锰作为催化剂,发生反应的化学方程式为:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;某同学为测定一瓶市售氯酸钾的纯度,进行了以下实验:
试计算药品中含氯酸钾的质量分数是多少?
分析 根据氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,然后结合题中的数据进行解答.
解答 解:根据质量守恒定律可知,生成氧气的质量为:5g+1g-4.08g=1.92g,
设参加反应的氯酸钾的质量为x,
2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑
245 96
x 1.92g
$\frac{245}{x}$=$\frac{96}{1.92g}$
x=4.9g
所以样品中含氯酸钾的质量分数为:$\frac{4.9g}{5g}$×100%=98%.
答:样品中含氯酸钾的质量分数为98%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
5.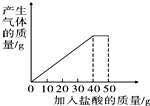 石灰石样品的主要成分是CaCO3(已知其他杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:
石灰石样品的主要成分是CaCO3(已知其他杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:
请计算:
(1)石灰石样品中杂质的质量为4g;
(2)所加盐酸的溶质质量分数.
(3)当加入稀盐酸质量为40克时,所得溶液的质量为48.96克.
 石灰石样品的主要成分是CaCO3(已知其他杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:
石灰石样品的主要成分是CaCO3(已知其他杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 10 | 10 | 10 |
| 剩余固体的质量/g | 16 | 12 | 8 |
(1)石灰石样品中杂质的质量为4g;
(2)所加盐酸的溶质质量分数.
(3)当加入稀盐酸质量为40克时,所得溶液的质量为48.96克.
12.日常生活中,下列做法正确的是( )
| A. | 电视机着火时用水浇灭 | |
| B. | 进入久未开启的菜窖用手电筒照明 | |
| C. | 用钢丝刷擦洗铝锅上的污垢 | |
| D. | 厨房天然气泄漏,立即关闭阀门并轻轻开窗通风 |
2.“车祸猛于虎,生命只一次”,今年五一假期多起车祸中发生的变化是化学变化的是( )
| A. | 玻璃破碎 | B. | 轮胎爆炸 | C. | 车轴断裂 | D. | 汽油燃烧 |
 化学与生活息息相关,可以帮助人类认识、改造世界.
化学与生活息息相关,可以帮助人类认识、改造世界.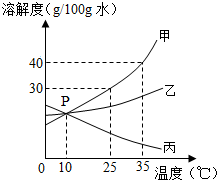 生活离不开水,水既普通又宝贵.
生活离不开水,水既普通又宝贵.