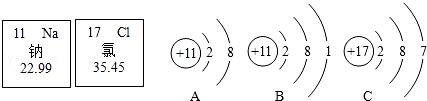题目内容
16.下列对分子、原子、离子的描述,其中错误的是( )| A. | 原子可以构成分子,原子也可以形成离子 | |
| B. | 分子之间有间隔,原子和离子之间没有间隔 | |
| C. | 分子和原子时电中性的,离子是带电的粒子 | |
| D. | 分子、原子、离子都是构成物质的基本粒子 |
分析 A、根据分子、原子、离子的形成考虑;
B、构成物质的基本粒子是分子、原子和离子.微观粒子的质量和体积都很小,微粒之间有一定间隔,总是不断运动的
C、根据分子、原子、离子的电性考虑;
D、根据物质的构成考虑;
解答 解:A、原子可以构成分子,也可以通过得失电子形成离子,故对;
B、微观粒子之间都有一定间隔,该选项说法不正确;
C、分子和原子时电中性的,离子是带电的粒子,故C对;
D、有的物质是由分子构成,有的物质是由原子构成,有的物质是由离子构成,分子、原子、离子都是构成物质的基本粒子,故D对.
故选B.
点评 主要考查了原子的构成,离子的概念、分子的特点、物质的构成微粒,要熟记它们并能灵活运用.

练习册系列答案
相关题目
6.在一次化学实验中,同学们将饱和CuSO4溶液逐滴加到5mL饱和NaOH溶液中,观察到以下异常实验现象
(1)在实验①中同学们根据所学初中化学知识判断蓝色沉淀是Cu(OH)2,请你写出生成蓝色沉淀的化学方程式CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
(2)已知:Ⅰ.Cu(OH)2在室温下稳定,70℃~80℃时可脱水分解生成CuO;Ⅱ.酮酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色:
实验①中蓝色沉淀为什么消失?同学们继续进行如下探究:小陶认为蓝色沉淀消失可能是Cu(OH)2发生了分解,其他同学一致否定了他的猜测,理由是沉淀消失,形成亮蓝色溶液,而氢氧化铜分解产生的是黑色固体;
(3)同学们交流讨论后,提出以下两种猜想:猜想一:少许Cu(OH)2可溶于足量水中;猜想二:Cu(OH)2粉末(其它试剂可任选)设计如下实验,请你填写表中的空格
(4)根据实验,并进一步查阅资料知道,Cu(OH)2在浓NaOH溶液中溶解生成Na2Cu(OH)4,反应的化学方程式是Cu(OH)2+2NaOH=Na2Cu(OH)4;根据实验可知饱和CuSO4溶液与饱和NaOH溶液的反应是放热反应,依据的实验现象是资料Ⅰ显示Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO,而表格1可知随着氢氧化钠溶液的滴加,观察到产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色.
| 实验序号 | 滴加CuSO4溶液的量 | 实验现象 |
| ① | 第1-6滴 | 产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
| ② | 第7-9滴 | 产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色 |
(2)已知:Ⅰ.Cu(OH)2在室温下稳定,70℃~80℃时可脱水分解生成CuO;Ⅱ.酮酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色:
实验①中蓝色沉淀为什么消失?同学们继续进行如下探究:小陶认为蓝色沉淀消失可能是Cu(OH)2发生了分解,其他同学一致否定了他的猜测,理由是沉淀消失,形成亮蓝色溶液,而氢氧化铜分解产生的是黑色固体;
(3)同学们交流讨论后,提出以下两种猜想:猜想一:少许Cu(OH)2可溶于足量水中;猜想二:Cu(OH)2粉末(其它试剂可任选)设计如下实验,请你填写表中的空格
| 实验序号 | 实验方法与操作 | 实验现象 | 结论 |
| ③ | 将少许Cu(OH)2粉末加到5mL蒸馏水中, 充分振荡 | 沉淀不消失 | 猜想一错误 |
| ④ | 将少许Cu(OH)2粉末加到NaOH浓溶液中,充分振荡 | 沉淀消失,溶液变成亮蓝色 | 猜想二正确 |
7.在CO、CO2和N2的混合气体中,氧元素的质量分数为76%.将10克混合气体先通入灼热的氧化铁,再通入足量的石灰水中,最多可得到白色沉淀物的质量是( )
| A. | 10克 | B. | 20克 | C. | 30克 | D. | 40克 |
11.用过氧化氢和二氧化锰制取氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,据此填表.
| 项目 | 反应物 | 生成物 | |
| H2O2 | H2O | O2 | |
| 质量比 | 68 | 36 | 32 |
| A | 34g | 18g | 16g |
| B | 17g | 9g | 8g |
1.下列所示实验中不能达到实验目的是( )
| A. | 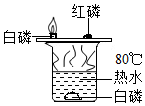 验证可燃物 燃烧的条件 | |
| B. | 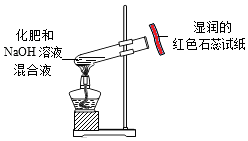 鉴别两种化肥: NH4Cl和KNO3 | |
| C. | 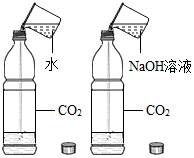 证明CO2与NaOH反应 | |
| D. | 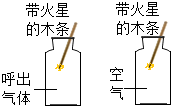 探究呼出气体和空气中 氧气的含量不同 |
 赣南脐橙享誉全国,如图标签所示为某品牌脐橙的营养成分.
赣南脐橙享誉全国,如图标签所示为某品牌脐橙的营养成分.
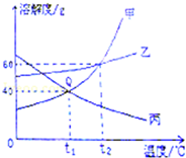 如图为甲、乙、丙三种固体物质的溶解度曲线图,请回答下列问题.
如图为甲、乙、丙三种固体物质的溶解度曲线图,请回答下列问题.