题目内容
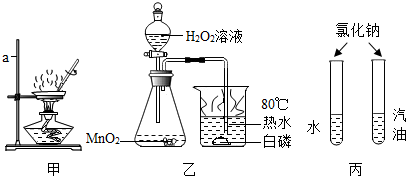
过氧化钠(Na2O2)是一种供氧剂,广泛用于潜水艇和防毒面具中.能与好H2O或CO2反应,产生O2.
(1)Na2O2中钠元素的化合价为 .
(2)Na2O2与CO2反应,除生成O2外还生成一种物质,该物质的水溶液可以使无色酚酞变红.该物质的化学式为 ,属于氧化物、酸、碱、盐中的 类.
(3)Na2O2与水反应的方程式为2Na2O2+2H2O=4NaOH+O2↑请列式计算用该方法制取48g O2,需要Na2O2的质量.
(4)在过氧化钠与水反应得到的无色溶液中加入MnO2,发现又产生大量的气泡.说明在此反应过程中还产生了 (填化学式).
(1)Na2O2中钠元素的化合价为
(2)Na2O2与CO2反应,除生成O2外还生成一种物质,该物质的水溶液可以使无色酚酞变红.该物质的化学式为
(3)Na2O2与水反应的方程式为2Na2O2+2H2O=4NaOH+O2↑请列式计算用该方法制取48g O2,需要Na2O2的质量.
(4)在过氧化钠与水反应得到的无色溶液中加入MnO2,发现又产生大量的气泡.说明在此反应过程中还产生了
考点:有关元素化合价的计算,常见的氧化物、酸、碱和盐的判别,质量守恒定律及其应用,根据化学反应方程式的计算
专题:结合课本知识的信息
分析:(1)根据Na2O2中Na元素的化合价来计算氧元素的化合价;
(2)利用反应的化学方程式是2Na2O2+2CO2=O2+2X及质量守恒定律来推断X的化学式.
(3)据氧气的质量,并结合化学方程式计算过氧化钠的质量.
(4)考虑MnO2可作双氧水分解的催化剂.
(2)利用反应的化学方程式是2Na2O2+2CO2=O2+2X及质量守恒定律来推断X的化学式.
(3)据氧气的质量,并结合化学方程式计算过氧化钠的质量.
(4)考虑MnO2可作双氧水分解的催化剂.
解答:解:
(1)在Na2O2中Na元素的化合价为+1价,根据化合物中正负化合价的代数和为0,设氧元素的化合价为x,则(+1)×2+x×2=0,解得x=-1;
(2)由反应的化学方程式是2Na2O2+2CO2=O2+2X,根据质量守恒定律可知,
反应前后的元素种类、原子的种类和个数不变,
反应前共4个Na原子、2个C原子、8个O原子,
则反应应后共4个Na原子、2个C原子、8个O原子,因生成物中氧分子含有2个O原子,
则X中共4个Na原子、2个C原子、6个O原子,又X的化学计量数为2,则X的化学式为Na2CO3;
(3)解:设需要过氧化钠的质量为x
2Na2O2+2H2O═4NaOH+O2↑
156 32
x 48g
则
=
,解得x=234g
答:若用过氧化钠(Na2O2)为原料制取相同质量的氧气,需要234g的过氧化钠;
(4)在过氧化钠与水反应得到的无色溶液中加入MnO2,发现又产生大量的气泡.说明在此反应过程中还产生了 H2O2.
故答案为:
(1)-1; (2)Na2CO3; 盐;(3)234g;(4)H2O2
(1)在Na2O2中Na元素的化合价为+1价,根据化合物中正负化合价的代数和为0,设氧元素的化合价为x,则(+1)×2+x×2=0,解得x=-1;
(2)由反应的化学方程式是2Na2O2+2CO2=O2+2X,根据质量守恒定律可知,
反应前后的元素种类、原子的种类和个数不变,
反应前共4个Na原子、2个C原子、8个O原子,
则反应应后共4个Na原子、2个C原子、8个O原子,因生成物中氧分子含有2个O原子,
则X中共4个Na原子、2个C原子、6个O原子,又X的化学计量数为2,则X的化学式为Na2CO3;
(3)解:设需要过氧化钠的质量为x
2Na2O2+2H2O═4NaOH+O2↑
156 32
x 48g
则
| 156 |
| x |
| 32 |
| 48g |
答:若用过氧化钠(Na2O2)为原料制取相同质量的氧气,需要234g的过氧化钠;
(4)在过氧化钠与水反应得到的无色溶液中加入MnO2,发现又产生大量的气泡.说明在此反应过程中还产生了 H2O2.
故答案为:
(1)-1; (2)Na2CO3; 盐;(3)234g;(4)H2O2
点评:本题注重了化学的实际应用性,学生可利用信息中物质的化学式和反应方程式,结合化合价原则及质量守恒定律来分析解答.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
下能区分氮气和二氧化碳的方法是( )
| A、闻气味 |
| B、分别通入澄清石灰水 |
| C、观察颜色 |
| D、分别伸人燃着的木条 |
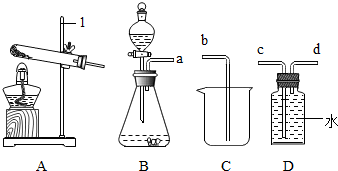 如图是实验室制取气体的装置.请根据要求回答:
如图是实验室制取气体的装置.请根据要求回答: