题目内容
将Cu-Zn合金样品20g放入足量稀硫酸中,所产生氢气的质量与反应时间的关系如下图所示。
试计算:
(1)原样品中所含锌的质量。
(2)实验测得20g该样品与154.7g某稀硫酸恰好完全反应,求此时所得溶液中溶质的质量分数。
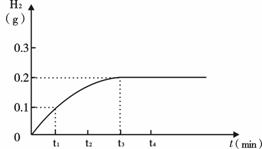
解:设原样品中锌的质量为x,生成ZnSO4的质量为y,则:
Zn+H2SO4 =ZnSO4 + H2↑ ……1分
65 161 2
x y 0.2g ……1分
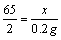 x=6.5g ……1分
x=6.5g ……1分
 y=16.1g ……1分
y=16.1g ……1分
反应后溶液的质量为:154.7g+6.5g-0.2g=161g……2分
溶液中溶质的质量分数为: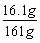 ×100%=10%……2分
×100%=10%……2分
答:原样品中锌的质量为6.5g,反应后溶液中溶质的质量分数为10%。

合金在生活中应用十分广泛。已知某合金粉末除含铝外,还含有铁、铜中的一种或两种。小明利用下图装置对合金粉末中铁、铜的存在进行探究时,误把氢氧化钠溶液当成稀硫酸加入到锥形瓶中,他惊奇的发现有无色气体放出,注射器活塞向右移动。
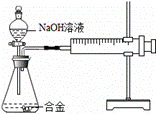
【提出疑问】
难道NaOH溶液也能与某些金属发生化学反应吗?
【查阅资料】
(1)铝能与氢氧化钠溶液反应,铁、铜不能与氢氧化钠溶液反应。
(2)铝与氢氧化钠溶液反应的化学方程式为:
2Al+2NaOH+2H2O═2NaAlO2+3H2↑(NaAlO2 溶于水,溶液显无色)
【进行猜想】
猜想1:该合金粉末除铝外,还含有铁。
猜想2:该合金粉末中除铝外,还含有 。
猜想3:该合金粉末中除铝外,还含有铁、铜。
【实验探究】
下列实验仅供选用的试剂:20%的硫酸溶液、30%的NaOH溶液。实验记录如下:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取一定量的合金粉末,加过量的 ,充分反应后过滤,滤渣备用 | 粉末部分溶解,并有无色气体放出 | 合金中一定含有
|
| ②取步骤①所得滤渣,加过量的____,充分反应 | 滤渣部分溶解,并有无色气体放出,溶液呈浅绿色 | 合金中一定含有
|
【交流反思】
1.一般来说,活泼金属能与稀硫酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质。铝与稀硫酸反应的化学方程式是__________________________。
2.若小明一开始向合金粉末中加入的是足量的稀硫酸,则最终剩余的固体成分是 。
【后续探究】
小明找到一块废旧的镁铝合金,积极探究其组成。他取32g铝镁合金样品,将120g氢氧化钠溶液平均分成三份依次加入样品中(2Al+2NaOH+2H2O═2NaAlO2+3H2↑,镁与氢氧化钠溶液不反应),充分反应后,过滤出固体,将其洗涤、干燥、称量,得实验数据如下:
| 所加氢氧化钠溶液的次数 | 第一次 | 第二次 | 第三次 |
| 剩余固体的质量/g | 21.2 | 10.4 | 8.0 |
计算:(1)该合金中,铝元素与镁元素的质量比是____________。
(2)所用氢氧化钠溶液中溶质的质量分数。(写出计算过程)
下表除去杂质的方法中,正确的是
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | Cu(NO3)2溶液(AgNO3) | 加过量铜粉,过滤 |
| B | KCl溶液(CaCl2) | 加适量Na2CO3溶液,过滤 |
| C | Fe(Zn) | 加足量稀盐酸,过滤 |
| D | CO(CO2) | 通过灼热的氧化铜粉末 |
已知金属R与硫酸铜溶液反应的化学方程式是:R+CuSO4=Cu+RSO4。则下列说法正确的是 ( )
A.该反应属于复分解反应 B.金属R的活泼性比Cu要强
C.该金属可能是金属铝 D.该金属一定是铁
根据下列五种微粒的结构示意图,所作出的判断中不正确的是
 |
A. 图中微粒共能表示3种元素 B. 图中表示的粒子属阴离子是③
C. 图中①、②两种微粒可构成A2B2型分子 D. 图中②和③两种微粒的化学性质相似
下列实验或实验操作正确的是( )
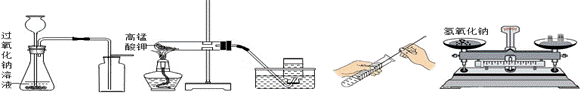
| A.过氧化氢制氧气 | B.高锰酸钾制氧气 | C.刷洗试管 | D.称量氢氧化钠固体 |
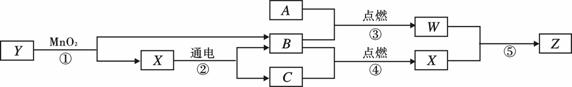
 式 ,该反应属于四种基本
式 ,该反应属于四种基本 反应类型中的
反应类型中的