题目内容
3.如图是粗盐提纯的主要操作,其中正确的是( )| A. | 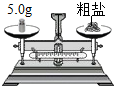 称量5.0g粗盐 | B. | 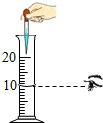 量取10mL水 | C. | 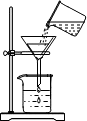 过滤 | D. | 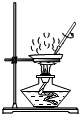 蒸发滤液 |
分析 A、根据托盘天平的使用要遵循“左物右码”的原则进行分析判断.
B、根据使用胶头滴管滴加少量液体的方法进行分析判断.
C、过滤液体时,注意“一贴、二低、三靠”的原则.
D、根据蒸发操作的注意事项进行分析判断.
解答 解:A、托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,图中所示操作错误.
B、使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到试管内或接触试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图中所示操作错误.
C、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流、漏斗下端没有紧靠在烧杯内壁上,图中所示操作错误.
D、蒸发时,应用玻璃棒不断搅拌,以防液体受热不均匀,造成液体飞溅,图中所示操作正确.
故选:D.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
13.下列对意外事故处理的方法错误的是( )
| A. | 扑灭森林火灾时,可设置隔离带 | |
| B. | 酒精在桌子上燃烧时用湿抹布盖灭 | |
| C. | 闻到煤气泄漏时开灯检查 | |
| D. | 炒菜时,油锅着火,应立即用锅盖盖灭 |
14.物质的俗名与化学式相对应不正确的是( )
| A. | 水银:Hg | B. | 熟石灰:CaO | C. | 烧碱:NaOH | D. | 纯碱:Na2CO3 |
8.下列相关事实用微观粒子的知识解释错误的是 ( )
| 事 实 | 解 释 | |
| A | 湿衣服晾干 | 水分子不断运动 |
| B | 蔗糖溶液不导电 | 蔗糖溶液中没有自由移动的带电粒子 |
| C | 盐酸、稀硫酸具有相似化学性质 | 都含有相同的氢元素 |
| D | 热胀冷缩 | 粒子之间的间隔受热增大,遇冷减小 |
| A. | A | B. | B | C. | C | D. | D |
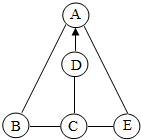 如图所示,B、D为黑色粉末,A在农业上可以用来配制农药波尔多液,c和E发生中和反应,并且产生白色沉淀.用“---“表示两种物质之间能发生化学反应,用“→“表示一种物质可抖转化为另一种物质.请回答下列问题;
如图所示,B、D为黑色粉末,A在农业上可以用来配制农药波尔多液,c和E发生中和反应,并且产生白色沉淀.用“---“表示两种物质之间能发生化学反应,用“→“表示一种物质可抖转化为另一种物质.请回答下列问题; 如图为大家经常使用的某品牌修正液标签上的部分文字和图片.请分析、推测该修正液的性质(至少答出三点):
如图为大家经常使用的某品牌修正液标签上的部分文字和图片.请分析、推测该修正液的性质(至少答出三点):