题目内容
11.碳酸钙是牙膏中一种常用的摩擦剂,可用石灰水作原料来制备,某工厂为了测定一批石灰石中所含碳酸钙的质量分数,称取1000g石灰石中样品(样品中的杂质不参加反应),磨成粉末后,放在电炉上高温锻烧至质量不再发生变化,冷却,称量剩余固体的质量为648g.据此计算:(1)生成二氧化碳的质量;
(2)石灰石样品中碳酸钙的质量分数.
分析 碳酸钙高温分解生成氧化钙和二氧化碳,根据质量守恒定律,混合物减少的质量即生成的二氧化碳质量,由反应的化学方程式,列式计算出参加反应的碳酸钙的质量,进而计算出石灰石样品中碳酸钙的质量分数.
解答 解:(1)由质量守恒定律,生成二氧化碳的质量为1000g-648g=352g.
(2)设参加反应的碳酸钙的质量为x
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 44
x 352g
$\frac{100}{44}=\frac{x}{352g}$ x=800g
石灰石样品中碳酸钙的质量分数为$\frac{800g}{1000g}$×100%=80%.
答:(1)生成二氧化碳的质量为352g;
(2)石灰石样品中碳酸钙的质量分数为80%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出二氧化碳的质量是正确解答本题的前提和关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下列物质的名称、俗名、化学式三者表示同一种物质的是( )
| A. | 水、干冰、CO2 | B. | 氢氧化钠、火碱、NaOH | ||
| C. | 碳酸钠、烧碱、Na2CO3 | D. | 氧化钙、熟石灰、CaO |
19.化学式一门以实验为基础的学科,化学实验室学习化学的重要方式,下图是粗盐提纯实验的部分操作,其中操作错误的是( )
| A. | 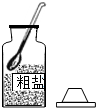 取一定量粗盐 | B. | 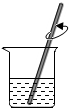 溶解 | C. | 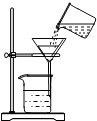 过滤 | D. | 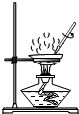 蒸发 |
6.化学兴趣小组同学发现实验台上按如下顺序摆放着7瓶不同的无色溶液(如图所示),其中4、5号试剂瓶标签破损.

【提出问题】这两瓶试剂分别是什么?
【查阅资料】
①碱性的亚硫酸钠(Na2SO3)溶液、Na2CO3溶液都能与中性的CaCl2溶液发生复分解反应,产生白色沉淀.
②Na2SO3+2HCl═2NaCl+SO2↑+H2O.
③CO2与SO2均可以使澄清石灰水变浑浊,SO2是一种有刺激性气味的气体.
【作出猜想】4、5号溶液可能分别是NaOH、Na2CO3、Na2SO3或NaCl溶液中的一种.
【实施方案】取少量4、5号溶液分别于试管中,然后分别进行下列三组实验.
实验1:在两支试管中分别滴入上述七种溶液中的1,两试管中的溶液均变成红色,说明4、5号溶液均不可能是上述猜想中的NaCl(或氯化钠)溶液.
实验2:在两支试管中分别滴入上述七种溶液中的3号溶液,两试管中均产生白色沉淀,4、5号溶液可能分别是NaS2O3溶液和Na2CO3溶液中的一种.写出其中一个反应的化学方程式Na2CO3+Ca(OH)2═CaCO3↓+2NaOH(或Na2SO3+Ca(OH)2═CaSO3↓+2NaOH).
实验3:在两支试管中分别滴入上述七种溶液中的2号溶液,在盛4号溶液的试管中有无色无味气体产生现象,说明4号是Na2CO3溶液;在盛5号溶液的试管中有刺激性气味的气体产生现象,说明5号是Na2SO3溶液.
【实验反思】同学们经过分析,认为4号溶液还可能是变质的NaOH溶液.请你利用上述图中的试剂设计鉴定实验方案,完成实验报告.

【提出问题】这两瓶试剂分别是什么?
【查阅资料】
①碱性的亚硫酸钠(Na2SO3)溶液、Na2CO3溶液都能与中性的CaCl2溶液发生复分解反应,产生白色沉淀.
②Na2SO3+2HCl═2NaCl+SO2↑+H2O.
③CO2与SO2均可以使澄清石灰水变浑浊,SO2是一种有刺激性气味的气体.
【作出猜想】4、5号溶液可能分别是NaOH、Na2CO3、Na2SO3或NaCl溶液中的一种.
【实施方案】取少量4、5号溶液分别于试管中,然后分别进行下列三组实验.
实验1:在两支试管中分别滴入上述七种溶液中的1,两试管中的溶液均变成红色,说明4、5号溶液均不可能是上述猜想中的NaCl(或氯化钠)溶液.
实验2:在两支试管中分别滴入上述七种溶液中的3号溶液,两试管中均产生白色沉淀,4、5号溶液可能分别是NaS2O3溶液和Na2CO3溶液中的一种.写出其中一个反应的化学方程式Na2CO3+Ca(OH)2═CaCO3↓+2NaOH(或Na2SO3+Ca(OH)2═CaSO3↓+2NaOH).
实验3:在两支试管中分别滴入上述七种溶液中的2号溶液,在盛4号溶液的试管中有无色无味气体产生现象,说明4号是Na2CO3溶液;在盛5号溶液的试管中有刺激性气味的气体产生现象,说明5号是Na2SO3溶液.
【实验反思】同学们经过分析,认为4号溶液还可能是变质的NaOH溶液.请你利用上述图中的试剂设计鉴定实验方案,完成实验报告.
| 实验操作 | 实验现象 | 实验结论 |
| 1取少量4号溶液于试管中, 加入足量CaCl2溶液,过滤. 2向滤液中滴加1号溶液 | 1溶液产生白色沉淀 2溶液由无色变成红色 | 4号溶液时部分变质的NaOH溶液 |
7.甲、乙、丙、丁四位同学用锌与稀硫酸反应,所得相关数据记录如表(实验中的误差忽略不计),计算:Zn+H2SO4═ZnSO4+H2↑
(1)甲同学加入金属锌的质量X’
(2)稀硫酸中溶质的质量分数
(1)甲同学加入金属锌的质量X’
(2)稀硫酸中溶质的质量分数
| 甲 | 乙 | 丙 | 丁 | |
| 取用稀硫酸质量/克 | 100 | 100 | 100 | 200 |
| 加入金属的质量/克 | X | 1.25X | 2X | 2X |
| 生成氢气的质量/克 | 0.4 | 0.5 | 0.6 | 0.8 |
 从图实验可得出铁生锈与H2O、O2(填化学式)有关.铁栏杆最常用的防锈措施是刷漆.其实铁锈还可以“回炉”重新制成铁,若将其用于工业炼铁,其基本原理是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2(填化学方程式),该反应不属于(填“属于”或“不属于”)置换反应.
从图实验可得出铁生锈与H2O、O2(填化学式)有关.铁栏杆最常用的防锈措施是刷漆.其实铁锈还可以“回炉”重新制成铁,若将其用于工业炼铁,其基本原理是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2(填化学方程式),该反应不属于(填“属于”或“不属于”)置换反应. 2011年两会期间,政协委员们领到了会议通知、日程表、便签纸等东西都是采用“石头纸”.全国“两会”首次使用环保易降解的“石头纸”,体现了低碳生活的理念.“石头纸”的主要原料为碳酸钙,其外观与普通纸相似.
2011年两会期间,政协委员们领到了会议通知、日程表、便签纸等东西都是采用“石头纸”.全国“两会”首次使用环保易降解的“石头纸”,体现了低碳生活的理念.“石头纸”的主要原料为碳酸钙,其外观与普通纸相似. 
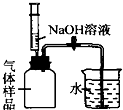 据报道:某农民为保鲜吃剩下的半个西瓜,将其送入菜窖时因CO2含量过高而导致死亡.某同学看了报道后,决定对自家菜窖内CO2的含量进行探究.
据报道:某农民为保鲜吃剩下的半个西瓜,将其送入菜窖时因CO2含量过高而导致死亡.某同学看了报道后,决定对自家菜窖内CO2的含量进行探究.