题目内容
8.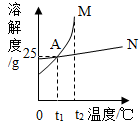 如图是M、N两种固体物质(不含结晶水)的溶解度曲线,下列说法错误的是( )
如图是M、N两种固体物质(不含结晶水)的溶解度曲线,下列说法错误的是( )| A. | 图中A点表示M、N两种物质在tl℃时溶解度相等 | |
| B. | t2℃时,分别将M、N饱和溶液冷却到tl℃,所得溶液 的 溶质质量分数都为25% | |
| C. | M中含有少量N,通常采用冷却结晶的方法提纯M | |
| D. | t1℃时,M的溶液恒温蒸发10g水析出lg晶体,再恒温蒸发20g水将析出5g晶体 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、通过分析溶解度曲线可知,图中A点表示M、N两种物质在tl℃时溶解度相等,故A正确;
B、t2℃时,M、N的溶解度是25g,所得溶液的溶质质量分数为:$\frac{25g}{125g}$×100%=20%,故B错误;
C、M物质的溶解度受温度影响较大,所以M中含有少量N,通常采用冷却结晶的方法提纯M,故C正确;
D、t1℃时,M物质的溶解度是25g,所以M的溶液恒温蒸发10g水析出lg晶体,溶液变成不会溶液,再恒温蒸发20g水将析出5g,故D正确.
故选:B.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.下列实验中利用提供的方案不能达到目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 检验某食物中是否含有淀粉 | 将碘液滴入食物样品中,看是否变蓝色 |
| B | 区分SO2和CO2两种气体 | 将气体通入高锰酸钾溶液,观察是否褪色 |
| C | 测某溶液的酸碱度 | 滴入酚酞试液,观察溶液颜色的变化 |
| D | 除去固体氯化钾中少量的二氧化锰 | 加水溶解后,过滤,蒸发 |
| A. | A | B. | B | C. | C | D. | D |
16.大多数不粘锅的内壁上都涂有一层聚四氟乙烯的涂层,其化学式可以表示为(CF2CF2)m(m为正整数).下列关于聚四乙烯的说法正确的是( )
| A. | 该物质是一种遇热不稳定的有机化合物 | |
| B. | 该物质受热后易发生化学变化 | |
| C. | 该物质的相对分子质量为100 | |
| D. | 该物质含氟的质量分数为76% |
3.国家新版《生活用水标准》中新增了一氯胺(NH2Cl)作为消毒剂,下列关于一氯胺的说法正确的是( )
| A. | 一氯胺是一种有机物 | |
| B. | 一氯胺的相对分子质量为51.5g | |
| C. | 一氯胺中各元素的质量分数最高的是Cl | |
| D. | 一氯胺由氮原子、氢分子和氯原子构成 |
13.下表列出了除去物质中所含少量杂质的方法,其中正确的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | CO2 | HCl | 依次通过足量的NaOH溶液和浓硫酸 |
| B | FeSO4溶液 | CuSO4 | 加入足量的锌粒,充分反应,过滤 |
| C | NaCl溶液 | Na2CO3 | 加入适量的澄清石灰水,过滤 |
| D | KCl | MnO2 | 加水充分溶解,过滤,蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
17. 屠呦呦因发现青蒿素(C15H22O5)荣获诺贝尔奖.青蒿素组成元素在元素周期表中的信息如图所示.下列说法正确的是( )
屠呦呦因发现青蒿素(C15H22O5)荣获诺贝尔奖.青蒿素组成元素在元素周期表中的信息如图所示.下列说法正确的是( )
 屠呦呦因发现青蒿素(C15H22O5)荣获诺贝尔奖.青蒿素组成元素在元素周期表中的信息如图所示.下列说法正确的是( )
屠呦呦因发现青蒿素(C15H22O5)荣获诺贝尔奖.青蒿素组成元素在元素周期表中的信息如图所示.下列说法正确的是( )| A. | 青蒿素属于有机高分子化合物 | |
| B. | 青蒿素由15个C、22个H和5个O原子构成 | |
| C. | 三种元素的本质区别是相对原子质量不同 | |
| D. | 青蒿素中氧元素的质量分数为28.37% |
18.在硝酸根、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色.有关判断正确的是( )
| A. | 滤渣中一定有银,没有铜和锌 | |
| B. | 滤渣中一定有银和锌,可能有铜 | |
| C. | 滤液中一定有硝酸锌、硝酸铜,可能有硝酸银 | |
| D. | 滤液中一定有硝酸锌、硝酸铜、硝酸银 |
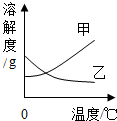
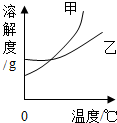
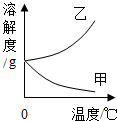
 在20℃和40℃时,分别向100g水中加入相同质量的甲和乙,充分溶解后的现象如图所示.下列图象中能正确表示甲、乙的溶解度随温度变化趋势的是( )
在20℃和40℃时,分别向100g水中加入相同质量的甲和乙,充分溶解后的现象如图所示.下列图象中能正确表示甲、乙的溶解度随温度变化趋势的是( )