题目内容
18.宁波轨道交通1号线为东西向主干线,西连高桥镇,东连北仑中心区,预计2014年6月竣工.在施工建设中,为将短轨连成长轨,工人常用点燃铝和氧化铁(Fe2O3)的混合物反应时放出大量的热,进行焊接铁轨中的缝隙,并生成氧化铝和熔融状态下的铁.反应的化学方程式为Fe2O3+2Al$\frac{\underline{\;点燃\;}}{\;}$Al2O3+2Fe,反应的基本类型是置换反应.分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可,根据置换反应的定义进行解答.
解答 解:点燃铝和氧化铁(Fe2O3)的混合物生成氧化铝和熔融状态下的铁,反应的化学方程式为:2Al+Fe2O3$\frac{\underline{\;点燃\;}}{\;}$2Fe+Al2O3;该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,故属于置换反应;
故答案为:
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
8.通过下列实验操作和现象得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 用黄铜片在铜片上刻画 | 铜片上出现明显痕迹 | 铜的硬度比黄铜大 |
| B | 50℃时,将17gKCl固体加入50g蒸馏水中,完全溶解后缓慢降温 | 降温至20℃时开始有晶体析出 | 20℃时KCl的溶解度为17g |
| C | 将白磷浸没在热水中,再向热水中通氧气 | 通氧气前白磷不燃烧,通氧气后白磷燃烧 | 氧气是燃烧的条件之一 |
| D | 点燃从导管放出的某气体,在火焰上方罩一个干而冷的烧杯 | 烧杯内壁有水珠产生 | 该气体是H2 |
| A. | A | B. | B | C. | C | D. | D |
9. 某科学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示),他们对此产生了兴趣.
某科学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示),他们对此产生了兴趣.
【提出问题】这瓶溶液究竟是什么?
经过询问实验老师得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
(1)小明根据标签上的组成元素认为一定不可能是NaCl.
(2)小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是这二者的化学式中Na元素的右下角不会有2.
为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验.
【设计实验】
【实验结论】
(3)该瓶无色溶液是Na2CO3.生成白色沉淀过程的化学方程式是_BaCl2+Na2CO3═BaCO3↓+2NaCl.
 某科学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示),他们对此产生了兴趣.
某科学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示),他们对此产生了兴趣.【提出问题】这瓶溶液究竟是什么?
经过询问实验老师得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
(1)小明根据标签上的组成元素认为一定不可能是NaCl.
(2)小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是这二者的化学式中Na元素的右下角不会有2.
为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验.
【设计实验】
| 实验操作 | 实验现象 |
| 取少量样品于试管中,慢慢滴加BaCl2溶液,静置一段时间, 倾去上层清液,向沉淀中继续滴加稀盐酸 | 先出现白色沉淀, 后产生大量气泡 |
(3)该瓶无色溶液是Na2CO3.生成白色沉淀过程的化学方程式是_BaCl2+Na2CO3═BaCO3↓+2NaCl.
13.2014年2月下旬,北仑“乌牛旱”茶叶开始采摘.为了保证茶叶的品质,茶叶包装要注意防潮,可在茶叶包装要注意防潮,可在茶叶包装中放入一小袋干燥剂,其成分为生石灰(CaO),则生石灰在物质分类上属于( )
| A. | 酸 | B. | 碱 | C. | 盐 | D. | 氧化物 |
3.肼(N2H4)是一种无色油状液体,有刺激性气味,有吸湿性.点燃时,迅速而完全燃烧,生成N2和H2O,并放出大量的热.下列关于N2H4的说法错误的是( )
| A. | 应密封保存 | B. | 完全燃烧的反应不属于置换反应 | ||
| C. | 可用作燃料 | D. | 生成N2和H2O的质量比为7:9 |
10.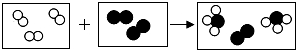 用“
用“ ”和“
”和“ ”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物质X,微观过程如图所示,下列说法正确的是( )
”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物质X,微观过程如图所示,下列说法正确的是( )
 用“
用“ ”和“
”和“ ”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物质X,微观过程如图所示,下列说法正确的是( )
”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物质X,微观过程如图所示,下列说法正确的是( )| A. | 在反应过程中各元素的化合价不变 | |
| B. | 该反应为置换反应 | |
| C. | 参加反应的A2与B2分子数之比为3:1 | |
| D. | 在反应过程中生成三种新物质 |
 图中A~I表示几种初中化学常见的物质,“→”表示物质间存在的转化关系,部分反应物、生成物及反应条件已略去.已知圈i中的转化均是分解反应.圈ⅱ中的转化均是化合反应.D和G是常见的非金属单质,组成化合物E和H的元素种类相同.组成化合物F和I的元素种类也相同,A常用来中和土壤的酸性.
图中A~I表示几种初中化学常见的物质,“→”表示物质间存在的转化关系,部分反应物、生成物及反应条件已略去.已知圈i中的转化均是分解反应.圈ⅱ中的转化均是化合反应.D和G是常见的非金属单质,组成化合物E和H的元素种类相同.组成化合物F和I的元素种类也相同,A常用来中和土壤的酸性.