题目内容
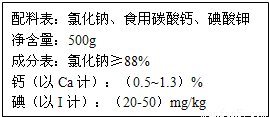
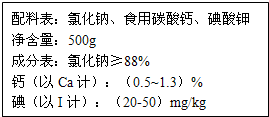 该图是某厂生产的加钙食盐包装标签上的部分文字说明,请仔细阅读并计算:为了测定此食盐中的钙元素含量,取10g这种食盐 溶于水,加入足量的稀盐酸,生成0.132g二氧化碳,请计算此加钙食盐中碳酸钙的质量分数.(注:成分中只有碳酸钙与盐酸反应)
该图是某厂生产的加钙食盐包装标签上的部分文字说明,请仔细阅读并计算:为了测定此食盐中的钙元素含量,取10g这种食盐 溶于水,加入足量的稀盐酸,生成0.132g二氧化碳,请计算此加钙食盐中碳酸钙的质量分数.(注:成分中只有碳酸钙与盐酸反应)分析:根据碳酸钙与盐酸反应的化学方程式和生成的二氧化碳的质量,即可计算出参与反应的碳酸钙的质量(即10g这种盐中碳酸钙的质量);然后再计算出此加钙食盐中碳酸钙的质量分数.
解答:解:设参与反应的碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 0.132g
=
解之得:x=0.3g,
此加钙食盐中碳酸钙的质量分数=
×100%=3%.
答:此加钙食盐中碳酸钙的质量分数为3%;
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 0.132g
| 100 |
| x |
| 44 |
| 0.132g |
解之得:x=0.3g,
此加钙食盐中碳酸钙的质量分数=
| 0.3g |
| 10g |
答:此加钙食盐中碳酸钙的质量分数为3%;
点评:本题考查了根据化学方程式进行的有关计算,完成此题,可以依据化学方程式的有关基础计算进行.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
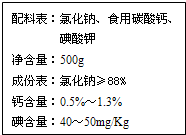 图是某厂生产的加钙碘盐包装袋商标的部分内容.请仔细阅读后回答以下问题:
图是某厂生产的加钙碘盐包装袋商标的部分内容.请仔细阅读后回答以下问题:
 该图是某厂生产的加钙食盐包装标签上的部分文字说明,请仔细阅读并计算:为了测定此食盐中的钙元素含量,取10g这种食盐 溶于水,加入足量的稀盐酸,生成0.132g二氧化碳,请计算此加钙食盐中碳酸钙的质量分数.(注:成分中只有碳酸钙与盐酸反应)
该图是某厂生产的加钙食盐包装标签上的部分文字说明,请仔细阅读并计算:为了测定此食盐中的钙元素含量,取10g这种食盐 溶于水,加入足量的稀盐酸,生成0.132g二氧化碳,请计算此加钙食盐中碳酸钙的质量分数.(注:成分中只有碳酸钙与盐酸反应)