题目内容
1.金属活性顺序在工农业生产和科学研究中都有重要作用,现有A、B、C三种金属,A、B可溶于盐酸,C不溶于盐酸,将A投入BCl2溶液中可发生反应:A+BCl2═ACl2+B.(1)A、B、C三者金属活动性由强到弱的顺序为A>B>C.
与金属置换反应规律相同,非金属单质之间的置换反应也有类似的规律,根据下列反应:
①Cl2+2NaBr═Br2+2NaCl,②Br2+2NaI═I2+2NaBr
(2)Cl2、Br2和I2单质的活泼性由强到弱的顺序为Cl2>Br2>I2.
(3)根据以上规律,下列反应可以发生的是a.
a.Cl2+2KI═2KCl+I2 b.2NaCl+I2═2NaI+Cl2↑
(4)经查阅资料,硫单质的活泼性比Cl2、Br2和I2都弱,请任写出一个化学方程式证明该结论I2+Na2S=S+2NaI.
分析 在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.据此分析判断回答有关的问题.
解答 解:(1)由题意可知,A、B可溶于盐酸,C不溶于盐酸,说明了金属的活动性是A、B大于C;由将A投入BCl2溶液中可发生反应:A+BCl2═ACl2+B,说明了金属的活动性是A大于B,由此可知,金属的活动性顺序是:A>B>C.
(2)由题意可知,与金属置换反应规律相同,非金属单质之间的置换反应也有类似的规律.由①Cl2+2NaBr═Br2+2NaCl可知,Cl2单质的活泼性大于Br2,由②Br2+2NaI═I2+2NaBr可知,Br2单质的活泼性大于I2.由此可知,Cl2、Br2和I2单质的活泼性由强到弱的顺序为:Cl2>Br2>I2.
(3)由于Cl2、Br2和I2单质的活泼性由强到弱的顺序为:Cl2>Br2>I2.所以反应Cl2+2KI═2KCl+I2 能发生,而反应2NaCl+I2═2NaI+Cl2↑不能发生.
(4)由于S的活动性比I2、Br2、Cl2都弱,所以应该选用最弱的一个进行实验.即选用碘单质和硫化钠等反应,反应的方程式是:I2+Na2S=S+2NaI.
故答为:(1)A>B>C;(2)Cl2>Br2>I2;(3)a;(4)I2+Na2S=S+2NaI.
点评 本题难度较大,主要考查了对金属活动性顺序的灵活应用,从而培养学生对知识的应变能力.

练习册系列答案
相关题目
11.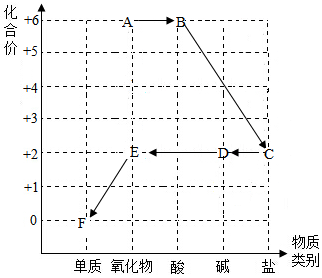 小科以化合价为纵坐标、以物质类别为横坐标绘制了如图,每种物质中都有一种元素的化合价与纵坐标的数值对应,图中字母均表示初中科学中的常见物质,其中“→”表示物质间的转化关系.已知A中氧元素的质量分数为60%,C、D、E、F均含有铜元素.下列说法不正确的是( )
小科以化合价为纵坐标、以物质类别为横坐标绘制了如图,每种物质中都有一种元素的化合价与纵坐标的数值对应,图中字母均表示初中科学中的常见物质,其中“→”表示物质间的转化关系.已知A中氧元素的质量分数为60%,C、D、E、F均含有铜元素.下列说法不正确的是( )
 小科以化合价为纵坐标、以物质类别为横坐标绘制了如图,每种物质中都有一种元素的化合价与纵坐标的数值对应,图中字母均表示初中科学中的常见物质,其中“→”表示物质间的转化关系.已知A中氧元素的质量分数为60%,C、D、E、F均含有铜元素.下列说法不正确的是( )
小科以化合价为纵坐标、以物质类别为横坐标绘制了如图,每种物质中都有一种元素的化合价与纵坐标的数值对应,图中字母均表示初中科学中的常见物质,其中“→”表示物质间的转化关系.已知A中氧元素的质量分数为60%,C、D、E、F均含有铜元素.下列说法不正确的是( )| A. | A的化学式为SO3 | B. | D是一种不溶性碱 | ||
| C. | 从E反应得到F是置换反应 | D. | F能与B的稀溶液不能发生化学反应 |
12.氧化铋俗称铋黄,是制作防火纸的材料之一.铋黄中铋元素(Bi)的化合价为+3价,则氧化铋的化学式是( )
| A. | BiO | B. | Bi3O2 | C. | Bi2O3 | D. | Bi2O5 |
9.化学在能源利用、环境保护等方面起着重要作用,下列做法错误的是( )
| A. | 变废为宝,将地沟油转化为航空燃油 | |
| B. | 城市道路使用太阳能景观灯,既节能又环保 | |
| C. | 为治理雾霾,禁止使用化石燃料 | |
| D. | 加强废旧金属的回收和再利用,有利于对环境的保护 |
13.空气成分中,可充入灯泡中制成霓虹灯的是气体是( )
| A. | 稀有气体 | B. | 二氧化碳 | C. | 氮气 | D. | 氧气 |
10.下列叙述、对应的化学方程式、所属基本反应类型都正确的是( )
| A. | 服用含氢氧化铝的药物治疗胃酸过多 Al(OH)3+3HCl=AlCl3+3H2O 复分解反应 | |
| B. | 拉瓦锡研究空气成分 2Hg0$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+02 分解反应 | |
| C. | 用天然气作燃料 CH4+O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 氧化反应 | |
| D. | 验证铜和铝的活动性 3Cu+A12(S04)3=3CuS04+2Al 置换反应 |
