题目内容
6.石英的主要成分为二氧化硅,其化学式为SiO2.它是玻璃工业和陶瓷工业的原料,冶金工业的助熔剂.用石英制备高纯硅的流程示意图如图: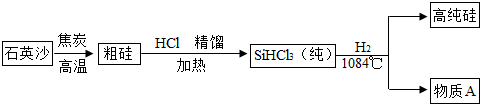
(1)二氧化硅属于氧化物(填“酸”、“碱”、“盐”、“氧化物”或“有机物”中一种).
(2)与碱反应时,SiO2和CO2有相似的化学性质.装NaOH溶液的试剂瓶不能用玻璃塞,是因为在常温下,NaOH与玻璃塞中的SiO2缓慢地反应,生成有粘性的硅酸钠,进而使瓶口与瓶塞粘合在一起的缘故.试写出该反应的化学方程式2NaOH+SiO2═Na2SiO3+H2O.
(3)硅是太阳能电池和电脑芯片不可缺少的材料.制备粗硅的反应为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,属于置换反应类型(填“分解”、“化合”、“置换”、“复分解”之一).
分析 (1)掌握氧化物的概念:由两种元素组成,一种为氧元素;
(2)了解装有氢氧化钠溶液的试剂瓶不能用玻璃塞的原因根据方程式的写法考虑;
(3)制备粗硅的反应为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,符合“单换单”,为置换反应.
解答 解:(1)二氧化硅由硅和氧两种元素组成,所以二氧化硅属于氧化物;
(2)NaOH与玻璃塞中的SiO2缓慢地发生反应生成Na2SiO3和H2O.所以不能用玻璃塞,该反应的反应物是氢氧化钠和二氧化硅,生成物是Na2SiO3和水,用观察法配平即可,所以该反应的化学方程式为2NaOH+SiO2=Na2SiO3+H2O;
(3)制备粗硅的反应为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,二氧化硅属于化合物,碳是单质,生成物中硅是单质,一氧化碳是化合物,一种单质和一种化合物反应生成另一种单质和另一种化合物属于置换反应.
故答案为:(1)氧化物;
(2)2NaOH+SiO2═Na2SiO3+H2O;
(3)置换.
点评 掌握氧化物的概念、反应类型的判定方法;掌握质量守恒定律的内容及其应用.知道使用碱溶液吸收氯化氢气体.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
14.碲(Te)被誉为“现代工业、国防与尖端技术的维生素,创造人间奇迹的桥梁”.实验室模拟提取碲的一个实验是:取某含碲溶液于烧瓶中,加入适量NaCl,加热到一定温度,持续通入SO2,待反应一定时间,过滤得到粗碲.
(1)反应的总化学方程式为:TeSO4+2SO2+3X$\frac{\underline{\;\;△\;\;}}{\;}$Te↓+3H2SO4,则X为H2O(填化学式).
(2)为探究获得较高粗碲沉淀率的反应条件,某研究小组在控制NaC1浓度和SO2流量不变的条件下,进行下述对比试验,数据如下:
①该小组研究的反应条件是温度和反应时间.
②实验a和b 的目的是比较相同时间,不同的反应温度对粗碲沉淀率的影响.
③在上述四组实验中,最佳的反应条件是80℃和2.0h.
④为了提升设备利用效率和节约能源,可进一步优化反应条件测定粗碲沉淀率.若再设计对比实验,选择的反应条件还可以是A(填选项).
A.80℃,1.5h B.80℃,2.5h C.70℃,2.0h D.95℃,2.0h.
(1)反应的总化学方程式为:TeSO4+2SO2+3X$\frac{\underline{\;\;△\;\;}}{\;}$Te↓+3H2SO4,则X为H2O(填化学式).
(2)为探究获得较高粗碲沉淀率的反应条件,某研究小组在控制NaC1浓度和SO2流量不变的条件下,进行下述对比试验,数据如下:
| 实验 | 温度/℃ | 反应时间/h | 粗蹄沉淀率/% |
| a | 65 | 3.0 | 65.0 |
| b | 80 | 3.0 | 98.9 |
| c | 80 | 2.0 | 98.9 |
| d | 90 | 2.0 | 97.0 |
②实验a和b 的目的是比较相同时间,不同的反应温度对粗碲沉淀率的影响.
③在上述四组实验中,最佳的反应条件是80℃和2.0h.
④为了提升设备利用效率和节约能源,可进一步优化反应条件测定粗碲沉淀率.若再设计对比实验,选择的反应条件还可以是A(填选项).
A.80℃,1.5h B.80℃,2.5h C.70℃,2.0h D.95℃,2.0h.
11.如图是某化学反应过程的模拟图,结合图示下列说法不正确的是( )


| A. | 该化学反应的基本类型属于分解反应 | |
| B. | 该反应可用化学方程式C2H5OH+3O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O 来表示 | |
| C. | 该反应揭示了物质发生化学反应前后元素种类相同,原子个数相等的规律 | |
| D. | 该反应中有元素的化合价发生了改变 |
15.以下是一些常用的危险品图标,装运浓硫酸、浓硝酸和浓盐酸都需要贴上的图标是( )
| A. |  爆炸性 | B. |  易燃性 | C. |  有毒性 | D. |  腐蚀性 |
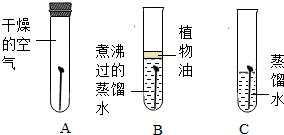 如图所示,A、B、C三支试管中的铁钉分别处于不同的环境.将它们放置一周时间,每天进行观察,发现C试管中的铁钉最易生锈.该实验表明,铁生锈实际上是铁跟氧气、水等物质相互作用,发生的一系列复杂的化学反应.
如图所示,A、B、C三支试管中的铁钉分别处于不同的环境.将它们放置一周时间,每天进行观察,发现C试管中的铁钉最易生锈.该实验表明,铁生锈实际上是铁跟氧气、水等物质相互作用,发生的一系列复杂的化学反应. ”表示氧原子,“
”表示氧原子,“ ”表示氢原子).
”表示氢原子).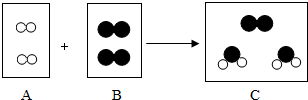
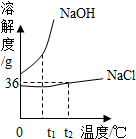 如图是氯化钠、氢氧化钠两种固体物质的溶解度曲线.
如图是氯化钠、氢氧化钠两种固体物质的溶解度曲线.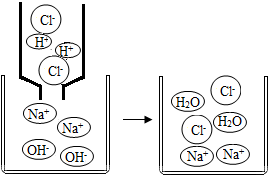 初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH-=H2O.像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式.离子方程式的书写一般按以下步骤:(以Na2SO4与BaCl2反应为例)
初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH-=H2O.像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式.离子方程式的书写一般按以下步骤:(以Na2SO4与BaCl2反应为例)