题目内容
19.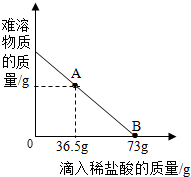 在一烧杯中盛有 21.2g CaCO3和 CaCl2的粉末状混合物,向其中加入 178.8g 水,使混合物中的可溶物完全溶解.然后再向其中逐滴加入溶质的质量分数为 20%的稀盐酸,烧杯中难溶固体物质的质量与所滴入稀盐酸的质量关系曲线如图所示:
在一烧杯中盛有 21.2g CaCO3和 CaCl2的粉末状混合物,向其中加入 178.8g 水,使混合物中的可溶物完全溶解.然后再向其中逐滴加入溶质的质量分数为 20%的稀盐酸,烧杯中难溶固体物质的质量与所滴入稀盐酸的质量关系曲线如图所示:请根据题意回答下列问题:
(1)在滴入稀盐酸的过程中,观察到的一条明显实验现象是:固体不断溶解,有气体产生.
(2)当滴入 20%的稀盐酸至图中 A 点时,烧杯中溶液里含有的溶质是CaCl2(写化学式).
(3)当滴入 20%的稀盐酸 73g 时(即 B 点),试通过计算,求此时烧杯中所得不饱和溶液中溶质的质量(计算结果精确至 0.1g).
分析 (1)根据碳酸钙和稀盐酸反应的现象,进行解答;
(2)根据碳酸钙和稀盐酸反应的方程式,及粉末状混合物的组成,进行分析解答;
(3)根据化学反应的方程式,计算出生成气体的质量,依据质量守恒定律即可求得烧杯中所得不饱和溶液的质量.
解答 解:(1)碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,所以在滴入稀盐酸的过程中,观察到的明显实验现象是:固体不断溶解,有气体产生;
(2)根据碳酸钙和稀盐酸反应的化学方程式,CaCO3+2HCl=CaCl2+CO2↑+H2O,当滴入20%的稀盐酸至图中A点时,烧杯中溶液里含有的溶质是:CaCl2;
(3)B点时滴入稀盐酸的质量为:73g×20%=14.6g
设生成CO2的质量为x
CaCO3+2HCl=CaCl2+CO2↑+H2O
73 44
14.6g x
$\frac{73}{14.6g}$=$\frac{44}{x}$
x=8.8g
烧杯中所得不饱和溶液的质量为:178.8g+21.2g+73g-8.8g=264.2g;
故答案为:(1)固体不断溶解,有气体产生;
(2)CaCl2;
(3)烧杯中所得不饱和溶液的质量为264.2g.
点评 溶液和化学反应融合的题目,是综合性的题型,要求比较高.通常学生在计算时常常会忽视了实际参加反应的是溶液中溶质的质量,这就要求学生足够细心、会分析、且条理分明.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.化学知识可以解决许多实际问题,如表中完全正确的一组是( )
| A. | 安全常识 | B. | 数据记录 |
| 天然气泄漏立即打开换气扇 炒菜时油锅着火-用锅盖盖灭 预防煤气中毒-确保烟道畅通 | 量筒量液体-体积为9.1ml 托盘天平称固体-质量为5.2g pH试纸测酸雨-pH为4.5 | ||
| C. | 物质的性质与用途 | D. | 化学反应的条件 |
| N2化学性质稳定-作保护气 H2具有可燃性-作气体燃料 CO具有还原性-冶炼金属 | 实验室制氧气-一定需要催化剂 燃烧-接触氧气,温度达到着火点 复分解反应-生成气体、沉淀或水 |
| A. | A | B. | B | C. | C | D. | D |
7.小波同学用实验方法区别稀盐酸和硫酸钠溶液(记作a、b),下列说法不正确的是( )
| A. | 向a、b两溶液中分别加入K2CO3溶液,则a中有无色气体产生 | |
| B. | 向a、b两溶液中分别加入Ba(NO3)2溶液,则b中会产生白色沉淀 | |
| C. | 常见物品如鸡蛋壳、金属铜,也可用来区别a、b | |
| D. | 上述选项中发生反应的均属复分解发生 |
14.下列微粒结构示意图中,说法错误的是( )
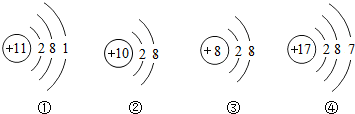
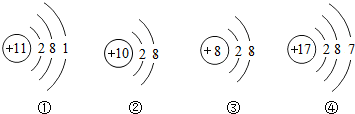
| A. | ①在化合物中的化合价通常为+1 价 | B. | ②的化学性质比较稳定 | ||
| C. | ③是一种阳离子 | D. | ④容易得到电子 |
12.下列实验操作正确的是( )
| A. | 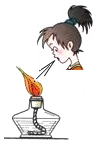 熄灭酒精灯 | B. | 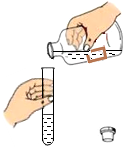 倾倒液体 | C. | 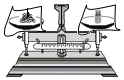 称量固体 称量固体 | D. | 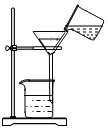 过滤 |
9.下列物质不属于空气污染物,不计入空气污染指数的项目是( )
| A. | CO2 | B. | CO | C. | NO2 | D. | 可吸入颗粒物 |