题目内容
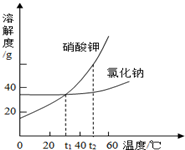 如图为氯化钠、硝酸钾两种物质的溶解度曲线.请根据图中内容回答下列问题:
如图为氯化钠、硝酸钾两种物质的溶解度曲线.请根据图中内容回答下列问题:(1)氯化钠和硝酸钾的饱和溶液在温度为
(2)在t1°C时,分别取两杯80mL水,各加入适量硝酸钾、氯化钠分别配成饱和溶液,将温度都升至t2°C时,若使溶液仍然是饱和溶液,则加入
(3)40℃时,20g 氯化钠溶于50g水中所形成的溶液是
(4)工业上将氯化钠和硝酸钾的热混合溶液(两者均己达到饱和)冷却至室温.析出晶体.
①析出的晶体中主要物质是
②关于剩余溶液.下列说法正确的是
A.只含氯化钠,不含硝酸钾,且氯化钠达到饱和 B.含有氯化钠,又含有硝酸钾,且只有氯化钠达到饱和
C.含有氯化钠,叉含有硝酸钾,且两者都达到饱和.
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)据饱和溶液中溶质的质量分数的计算式
×100%可知:溶解度相等则饱和溶液中溶质的质量分数相等;
(2)t1°C时二者的溶解度相等,则等质量的饱和溶液中溶质的质量相等,升温至t2°C时,硝酸钾的溶解度大于氯化钠的 溶解度,所以若使溶液仍然是饱和溶液,加入的硝酸钾的质量大于氯化钠;
(3)据该温度下氯化钠的溶解度分析解答;
(4)据硝酸钾和氯化钠的溶解度受温度影响情况分析解答.
| 溶解度 |
| 溶解度+100g |
(2)t1°C时二者的溶解度相等,则等质量的饱和溶液中溶质的质量相等,升温至t2°C时,硝酸钾的溶解度大于氯化钠的 溶解度,所以若使溶液仍然是饱和溶液,加入的硝酸钾的质量大于氯化钠;
(3)据该温度下氯化钠的溶解度分析解答;
(4)据硝酸钾和氯化钠的溶解度受温度影响情况分析解答.
解答:解:(1)据饱和溶液中溶质的质量分数的计算式
×100%可知:溶解度相等则饱和溶液中溶质的质量分数相等;而t1°C时氯化钠和硝酸钾的溶解度相等,所以饱和溶液溶质质量分数相等;
(2)t1°C时二者的溶解度相等,则等质量的饱和溶液中溶质的质量相等,升温至t2°C时,硝酸钾的溶解度大于氯化钠的 溶解度,所以若使溶液仍然是饱和溶液,加入的硝酸钾的质量大于氯化钠;
(3)由图可知:40℃时氯化钠的溶解度小于40g,即100g水中最多溶解氯化钠的质量小于40g,则20g 氯化钠溶于50g水中最多溶解的质量小于20g,所形成的溶液是 饱和溶液;
(4)①由于硝酸钾的溶解度受温度影响较大,氯化钠的溶解度受温度影响不大,且均随温度的降低而减小,所以工业上将氯化钠和硝酸钾的热混合溶液(两者均己达到饱和)冷却至室温,均会析出晶体.但氯化钠的溶解度随温度降低变化不大,硝酸钾的溶解度随温度降低减小幅度较大,所以析出的晶体主要是硝酸钾;
②关于剩余溶液.是氯化钠、硝酸钾的饱和溶液,故C正确;
故答案为:(1)t1°C;(2)硝酸钾;(3)饱和;(4)①硝酸钾;②C.
| 溶解度 |
| 溶解度+100g |
(2)t1°C时二者的溶解度相等,则等质量的饱和溶液中溶质的质量相等,升温至t2°C时,硝酸钾的溶解度大于氯化钠的 溶解度,所以若使溶液仍然是饱和溶液,加入的硝酸钾的质量大于氯化钠;
(3)由图可知:40℃时氯化钠的溶解度小于40g,即100g水中最多溶解氯化钠的质量小于40g,则20g 氯化钠溶于50g水中最多溶解的质量小于20g,所形成的溶液是 饱和溶液;
(4)①由于硝酸钾的溶解度受温度影响较大,氯化钠的溶解度受温度影响不大,且均随温度的降低而减小,所以工业上将氯化钠和硝酸钾的热混合溶液(两者均己达到饱和)冷却至室温,均会析出晶体.但氯化钠的溶解度随温度降低变化不大,硝酸钾的溶解度随温度降低减小幅度较大,所以析出的晶体主要是硝酸钾;
②关于剩余溶液.是氯化钠、硝酸钾的饱和溶液,故C正确;
故答案为:(1)t1°C;(2)硝酸钾;(3)饱和;(4)①硝酸钾;②C.
点评:本题主要考查了学生依据溶解度曲线、物质的溶解度概念等分析、解答问题的能力,难度不大.

练习册系列答案
相关题目
除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是( )
| A、CO2气体(CO气体)--通入氧气 |
| B、CaO固体(CaCO3固体)--加水充分溶解,过滤 |
| C、KCl固体(MnO2固体)--加水充分溶解,过滤,蒸发结晶 |
| D、除去铜粉中的木炭粉:将混合物在空气中充分灼烧 |
化学变化中一定有( )
| A、气体放出 | B、沉淀生成 |
| C、颜色变化 | D、有其他物质生成 |
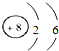 ,可知该原子的核电荷数为
,可知该原子的核电荷数为 如图所示是A、B、C三种固体物质的溶解度曲线,请根据图示回答.
如图所示是A、B、C三种固体物质的溶解度曲线,请根据图示回答.