题目内容
19.现有含Fe2O3为80%的赤铁矿石4000t,试计算:理论上利用这些赤铁矿石可炼出含铁为96%的生铁多少吨?分析 由赤铁矿石的质量、氧化铁的质量分数、生铁中铁的质量分数,根据赤铁矿炼铁的化学方程式可以列式计算出炼出生铁的质量.
解答 解:设理论上可以炼出含铁96%的生铁的质量为x.
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
4000t×80% 96%x
$\frac{160}{112}=\frac{4000t×80%}{96%x}$ 解得:x≈2333.3t
答:可炼出含铁96%的生铁2333.3t.
点评 本题难度不大,考查含杂质物质的化学方程式的计算,注意代入方程式计算的必须是纯物质的质量是正确解答此类题的关键

练习册系列答案
相关题目
7.下列属于合金的是 ( )
| A. | 硬铝 | B. | 赤铁矿 | C. | 足金 | D. | 氧化镁 |
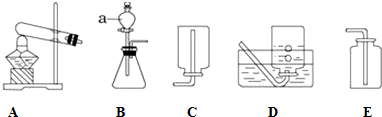
11.甲、乙、丙、丁四位同学在实验室里进行如下操作,其中正确的是( )
| A. | 甲做完实验后,将剩余的试剂倒回原试剂瓶 | |
| B. | 乙在点燃酒精灯时,用燃着的酒精灯引燃另一只酒精灯 | |
| C. | 丙在取稀盐酸时,在无用量说明的情况下,量取了1-2mL | |
| D. | 丁直接用手将粉末状药品加入试管中 |
8.图为甲、乙两种物质的溶解度曲线,从图中可获得正确信息的是( )
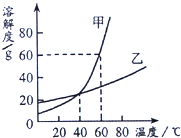

| A. | 40℃时,甲和乙物质的溶解度相同 | |
| B. | 升高温度可使不饱和的甲溶液变为饱和 | |
| C. | 60℃时,溶液甲的浓度大于乙 | |
| D. | 甲的溶解度大于乙的溶解度 |
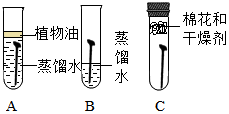 小林同学用相同的铁钉探究铁生锈与哪些因素有关,设计的实验如图.经过一周观察:试管A 和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀.根据上述描述请你完成:
小林同学用相同的铁钉探究铁生锈与哪些因素有关,设计的实验如图.经过一周观察:试管A 和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀.根据上述描述请你完成: