题目内容
 小明同学绘制了如图所示a、b、c三种固体物质的溶解度曲线,根据图象回答下列问题:
小明同学绘制了如图所示a、b、c三种固体物质的溶解度曲线,根据图象回答下列问题:(1)P点的含义是
(2)t2℃时,30g a物质加入到50g水中不断搅拌,能形成
(3)t2℃时,a、b、c三种物质的溶解度按由大到小的顺序排列是
(4)将t1℃时,a、b、c三种物质的饱和溶液温度升高到t2℃时,则三种溶液中溶质的质量分数大小关系是
A.c>a=b B.a=b>c
C.a>b>c D.b>a>c
(5)我国有许多盐碱湖,湖中溶有大量的NaCl和Na2CO3,那里的人们“冬天捞碱,夏天晒盐.”据此你认为图中
考点:固体溶解度曲线及其作用,结晶的原理、方法及其应用,溶质的质量分数、溶解性和溶解度的关系
专题:物质的分离、除杂、提纯与共存问题
分析:(1)根据曲线中交点的含义考虑:表示该温度下两种物质的溶解度相等;
(2)根据t2℃a物质的溶解度来分析:溶解度是指在该温度下,在100g溶剂里所溶解的溶质质量;
(3)根据某一温度时物质溶解度的比较方法考虑:在该温度下向上作垂线,与曲线的交点,在上边的溶解度就大;
(4)根据溶质质量分数的计算方法考虑:饱和溶液的容质质量分数::
×100%.
(5)根据冬天捞碱说明Na2CO3的溶解度随温度的变化较大分析;
(2)根据t2℃a物质的溶解度来分析:溶解度是指在该温度下,在100g溶剂里所溶解的溶质质量;
(3)根据某一温度时物质溶解度的比较方法考虑:在该温度下向上作垂线,与曲线的交点,在上边的溶解度就大;
(4)根据溶质质量分数的计算方法考虑:饱和溶液的容质质量分数::
| 溶解度 |
| 溶解度+100g |
(5)根据冬天捞碱说明Na2CO3的溶解度随温度的变化较大分析;
解答:解:
(1)曲线中交点表示该温度时两种物质的溶解度相等,所以t1℃温度时,a、c物质的溶解度相等,都是20g;
(2)t2℃a物质的溶解度为50g,即100g水中最多溶解50g,则50g水中最多溶解25g,所以30g a加入50g水中不断搅拌,有5g没溶解,故属于饱和溶液,溶液质量为50g+25g=75g;
(3)从t2℃向上做垂线,与曲线的交点在上面的溶解度就大,所以t2℃时它们的溶解度大小顺序是:a>b>c;
(4)饱和溶液的质量分数与溶解度有关,t1℃时a、b、c三种物质的溶解度是:b>a═c,将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,a和b的溶解度都变大,变为不饱和溶液,所以溶质质量分数不变,还是b>a,由于C升温后溶解度减小,会析出晶体,所以溶质质量分数减小了,所以最后三种溶液的溶质质量分数由大到小的关系是:b>a>c.
(5)由题意人们冬天捞碱,说明Na2CO3的溶解度随温度的变化较大,图中的a曲线与纯碱的溶解度曲线相似;
答案:
(1)t1℃时a和c的溶解度相等为20克
(2)75
(3)abc
(4)D
(5)a
(1)曲线中交点表示该温度时两种物质的溶解度相等,所以t1℃温度时,a、c物质的溶解度相等,都是20g;
(2)t2℃a物质的溶解度为50g,即100g水中最多溶解50g,则50g水中最多溶解25g,所以30g a加入50g水中不断搅拌,有5g没溶解,故属于饱和溶液,溶液质量为50g+25g=75g;
(3)从t2℃向上做垂线,与曲线的交点在上面的溶解度就大,所以t2℃时它们的溶解度大小顺序是:a>b>c;
(4)饱和溶液的质量分数与溶解度有关,t1℃时a、b、c三种物质的溶解度是:b>a═c,将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,a和b的溶解度都变大,变为不饱和溶液,所以溶质质量分数不变,还是b>a,由于C升温后溶解度减小,会析出晶体,所以溶质质量分数减小了,所以最后三种溶液的溶质质量分数由大到小的关系是:b>a>c.
(5)由题意人们冬天捞碱,说明Na2CO3的溶解度随温度的变化较大,图中的a曲线与纯碱的溶解度曲线相似;
答案:
(1)t1℃时a和c的溶解度相等为20克
(2)75
(3)abc
(4)D
(5)a
点评:通过回答本题知道了溶解度曲线表示的意义,知道了溶解度如何比较大小,饱和溶液溶质质量分数的影响因素,知道了交点表示的意义.

练习册系列答案
相关题目
欲证明生石灰(CaO)中含有石灰石的最简便的方法是( )
| A、加热 |
| B、加入澄清石灰水 |
| C、滴加稀盐酸 |
| D、加热并通入二氧化碳 |
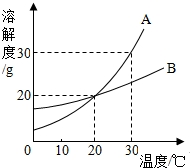 A、B两固体物质的溶解度曲线如图所示:
A、B两固体物质的溶解度曲线如图所示: 如图是实验室制取二氧化碳的一种装置.请回答下列问题;
如图是实验室制取二氧化碳的一种装置.请回答下列问题;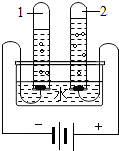 水是一种重要的自然资源,是生活、生产必不可少的物质.请回答下列问题:
水是一种重要的自然资源,是生活、生产必不可少的物质.请回答下列问题: 如图是A,B的溶解性曲线.将t1℃时的A,B的饱和溶液(溶液底部均没有剩余晶体)升温至t2℃时,此时两种溶液的溶质质量分数大小是A
如图是A,B的溶解性曲线.将t1℃时的A,B的饱和溶液(溶液底部均没有剩余晶体)升温至t2℃时,此时两种溶液的溶质质量分数大小是A